化学与社会生活息息相关,下列有关说法不正确的是( )
A. 沥青常用于铺路,可以通过石油分馏得到
B. 晨雾可以发生丁达尔效应
C. 氯气溶于水生成的次氯酸有强氧化性,可以起净水和杀菌消毒作用
D. 为提高人体对钙的有效吸收,医学上常以葡萄糖为原料合成补钙药物
C
【解析】A.沥青是石油分馏后剩余的固态烃,所以沥青可以通过石油分馏得到,故A正确;
B.晨雾是胶体,能发生丁达尔效应,故B正确;
C.次氯酸具有强氧化性只能杀菌消毒,不能净水,故C错误;
D.葡萄糖含-CHO,氧化转化为-COOH,最后可合成葡萄糖酸钙,则医药工业上,常以葡萄糖为工业原料合成补钙药物,故D正确;
故答案为C。
下列有关有机物的叙述错误的是( )
A. 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应
B. 异丙苯( ![]() )的一氯代物有5种
)的一氯代物有5种
C. 用碳酸钠溶液可一次性鉴别乙酸、苯和乙醇三种无色液体
D. 检验淀粉在稀硫酸催化条件下水解产物的方法:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热,观察是否出现砖红色沉淀
D
【解析】A.在溴化铁作催化剂条件下,Fe和液溴发生取代反应生成溴苯和HBr;在浓硫酸作催化剂、加热条件下,苯和浓硝酸发生取代反应生成硝基苯和水,二者都属于取代反应,故A正确;
B.异丙苯中都含有5种等效氢原子,其一氯代物有5种,故B正确;
C.乙酸和碳酸钠反应生成二氧化碳气体、苯和碳酸钠溶液互不相溶会分层、乙醇能溶于碳酸钠溶液而互溶,所以现象不同,可以鉴别,故C正确;
D.其水解产物和氢氧化铜发生氧化反应时必须在碱性条件下,所以在加入氢氧化铜悬浊液之前必须加入NaOH中和未反应的稀硫酸,否则得不到砖红色沉淀,故D错误;
故答案为D。
【点睛】“等效氢法”是判断烃的一元取代物的同分异构体最常用的方法。①分子中同一甲基上连接的氢原子等效,②同一碳原子所连的氢原子等效,同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效。
下列设计的实验方案能达到相应实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明“84”消毒液的氧化能力随溶液pH的减小而增强 | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 |
| B | 证明反应速率会随反应物浓度的增大而加快 | 用3mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL1mol•L-1CuSO4溶液,迅速产生较多气泡 |
| C | 证明碳和浓硫酸共热生成的气体中含有二氧化碳 | 将生成的气体直接通入澄清石灰水,有白色沉淀生成 |
| D | 浓盐酸与MnO2反应制备纯净 | 气体产物先通入浓硫酸,然后通过饱和食盐水 |
A. A B. B C. C D. D
A
【解析】A.同时加入食醋,生成HClO,可证明“84”消毒液的氧化能力随溶液pH的减小而增强,故A正确;
B.加入1mL 1mol•L-1CuSO4溶液,构成原电池,可加快反应速率,不能说明浓度对反应速率的影响,故B错误;
C.生成二氧化碳、二氧化硫均使石灰水变浑浊,由现象不能说明生成的气体中含有二氧化碳,故C错误;
D.浓盐酸与MnO2反应制得的氯气中混有挥发的HCl和水蒸气,则应先通过饱和食盐水除去HCl,后通过浓硫酸除去水,最终得到纯净的Cl2,故D错误;
故答案为A。
新型电池的开发与使用在现代社会中已很普遍,一种水煤气燃料电池的能量转化率可达90%以上。下列说法正确的是( )
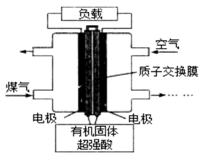
A. 该反应总反应式:CO+H2+O2=CO2+H2O
B. 电路中通过4mol电子,正极消耗112L空气
C. 有机固体中的H+ 在放电时向正极移动,造成正极pH减小
D. 若该电池的能量利用率为90%,则通入10mol水煤气(CO:H2 =1:1),则电路中可产生电子9mol
A
【解析】
【分析】
水煤气燃料电池的负极上通入的是燃料:一氧化碳和氢气,发生失电子的氧化反应,在正极上是氧气发生得电子的还原反应,阳离子移向正极,根据电极反应式确定电子转移的数目并进行计算即可。
【详解】A.一氧化碳和氢气,发生失电子的氧化反应,则水煤气燃料电池发生的总反应式为CO+H2+O2=CO2+H2O,故A正确;
B.电路中通过4 mol电子,正极消耗的是氧气,消耗氧气失1mol,消耗22.4 L×5=112L(标准状况)空气,选项中没有指明气体的状态,故B错误;
C.有机固体中的H+在放电时向正极移动,但是氧气在正极上得电子会消耗氢离子得到水,正极pH增大,故C错误;
D.负极电极反应为:H2-2e-═2H+、CO-2e-+H2O=CO2+2H+,若通入224L即10mol水煤气(CO:H2=1:1),转移电子是20mol,该电池的能量利用率为90%,则电路中可产生电子18mol,故D错误;
故答案为A。
设NA为阿伏加德罗常数值。关于常温下pH=2的H2C2O4 溶液,下列说法正确的是( )
A. 每升溶液中的H+数目为0.02NA
B. c(H+)=2c(C2O42-)+c(OH−)
C. 加水稀释使电离度增大,溶液pH增大
D. 加入NaHC2O4固体,溶液酸性增强
C
【解析】A.常温下pH=2的H2C2O4溶液中c(H+)=0.01mol/L,1L该溶液中含有的n(H+)=0.01mol/L×1L=0.01mol,含有H+数目为0.01NA,故A错误;
B.根据H2C2O4溶液中的电荷守恒可知:c(H+)=c(HC2O4-)+2c(C2O42-)+c(OH-),故B错误;
C.加水稀释c(H+)减小,温度不变,Kw不变,则依据Kw=c(H+)•c(OH-),可知c(OH-)浓度增大,溶液pH增大,故C正确;
D.草酸为弱电解质,第一步电离产生c(H+)与草酸氢根离子,加入加入NaHC2O4固体,增大草酸氢根离子浓度,平衡逆向移动,c(H+)浓度减少,溶液酸性减弱,故D错误;
故答案为。
本卷还有7题,登录并加入会员即可免费使用哦~

该作品由: 用户王其江分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。