次氯酸钠溶液和二氯异氰尿酸钠(C3N3O3Cl2Na)都是常用的杀菌消毒剂。 NaClO可用于制备二氯异氰尿酸钠.
(1)NaClO溶液可由低温下将Cl2缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为__________;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是__________________。
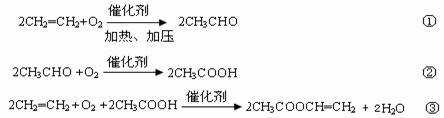
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为![]()
![]()
![]()
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用![]() Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品_______。(写出计算过程,![]() )
)
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值____________(填“偏高”或“偏低”)。
答案
(1). ![]() (2). NaClO溶液吸收空气中的CO2后产生HClO,HClO见光分解 (3).
(2). NaClO溶液吸收空气中的CO2后产生HClO,HClO见光分解 (3). ![]()
根据物质转换和电子得失守恒关系:![]()
得![]()
氯元素的质量:
![]()
该样品的有效氯为: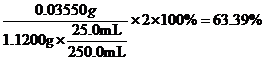
该样品的有效氯大于60%,故该样品为优质品 (4). 偏低
【解析】
【详解】(1) 由题意可知,氯气通入氢氧化钠中产生次氯酸钠,同时产生氯化钠,反应的离子方程式为:![]() ;次氯酸钠溶液长期暴露在空气中会吸收空气中的二氧化碳气体,因次氯酸酸性比碳酸弱,因此次氯酸钠可以与二氧化碳在水中反应产生HClO,HClO具有不稳定性,在受热或见光条件下会发生分解反应,产生HCl和O2,从而是次氯酸钠失效,故答案为:
;次氯酸钠溶液长期暴露在空气中会吸收空气中的二氧化碳气体,因次氯酸酸性比碳酸弱,因此次氯酸钠可以与二氧化碳在水中反应产生HClO,HClO具有不稳定性,在受热或见光条件下会发生分解反应,产生HCl和O2,从而是次氯酸钠失效,故答案为:![]() ;NaClO溶液吸收空气中的CO2后产生HClO,HClO见光分解;
;NaClO溶液吸收空气中的CO2后产生HClO,HClO见光分解;
(2) ①由题中反应可知,![]() 在酸性条件产生HClO,HClO氧化碘离子产生碘单质,碘单质再用硫代硫酸钠滴定,结合反应转化确定物质之间的关系为:
在酸性条件产生HClO,HClO氧化碘离子产生碘单质,碘单质再用硫代硫酸钠滴定,结合反应转化确定物质之间的关系为:![]() ,
, ![]() ,根据物质转换和电子得失守恒关系:得n(Cl)=0.5
,根据物质转换和电子得失守恒关系:得n(Cl)=0.5![]() =
=![]() ,
,
氯元素的质量:m(Cl)= ![]() =0.03550g,该样品中的有效氯为:
=0.03550g,该样品中的有效氯为: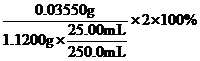 =63.39%,
=63.39%,
该样品中的有效氯大于60%,故该样品为优质品
故答案为:n(S2O![]() )=
)=![]() ,根据物质转换和电子得失守恒关系:
,根据物质转换和电子得失守恒关系:![]() ,得n(Cl)=0.5
,得n(Cl)=0.5![]() =
=![]() ,
,
氯元素的质量:m(Cl)= ![]() =0.03550g,该样品中的有效氯为:
=0.03550g,该样品中的有效氯为: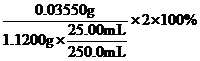 =63.39%,
=63.39%,
该样品中的有效氯大于60%,故该样品为优质品
②如果硫酸的用量过少,则导致反应![]() 不能充分进行,产生的HClO的量偏低,最终导致实验测得的有效氯含量会偏低,
不能充分进行,产生的HClO的量偏低,最终导致实验测得的有效氯含量会偏低,
故答案为:偏低;