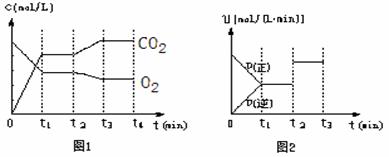
将一定量的SO2(g)和O2(g)分别通入容积为2 L的恒容密闭容器中,在不同温度下进行反应,得到表中的两组数据:
| 实验编号 | 温度 ℃ | 平衡常数 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||||||
| SO2 | O2 | SO2 | O2 | ||||||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 | ||||
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t | ||||
下列说法不正确的是( )
A.x=2.4
B.T1、T2的关系:T1>T2
C.K1、K2的关系:K2>K1
D.实验1在前6 min的反应速率v(SO2)=0.2 ![]() mol·L-1·min-1
mol·L-1·min-1
答案
.A 实验1从开始到反应达到化学平衡时,
2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
起始量/mol 4 2 0
变化量/mol 2.4 1.2 2.4
平衡量/mol x 0.8 2.4
故x=1.6,A项不正确;同样可以计算出y=0.2<0.8,而可逆反应正反应放热,故T1>T2,B项正确;温度越高,反应的平衡常数越小,故K2>K1,C项正确;用SO2表示的反应速率v(SO2)=![]() =0.2 mol·L-1·min-1,D项正确。
=0.2 mol·L-1·min-1,D项正确。


 ,
, ,所以
,所以