质子交换膜燃料电池(简称:PEMFC),又称固体高分子电解质燃料电池,是一种以含氢燃料与空气作用产生电力与热力的燃料电池,膜极组和集电板串联组合成一个燃料电池堆。目前,尤以氢燃料电池倍受电源研究开发人员的注目。它的结构紧凑,工作温度低(只有80℃),启动迅速,功率密度高,工作寿命长。工作原理如图,下列说法正确的是( )
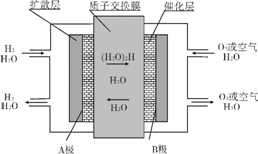
A. 可用一氧化碳、甲烷代替图中氢气和氧气(空气)形成质子交换膜燃料电池。
B. B极的电极反应式为:O2+4H++4e-=2H2O
C. 用该电池作为精炼铜的电源时,A极与粗铜电极相连
D. 当外电路中转移0.1mole−时,通过质子交换膜的H+的数目为0.2NA
答案
【答案】B
【解析】
【分析】
根据图知,该燃料电池中,氢气失电子生成氢离子,说明电解质溶液呈酸性,通入氢气的电极A是负极,负极反应式为2H2-4e-=4H+,通入氧气的电极B是正极,正极电极反应式为O2+4H++4e-=2H2O,电子从负极沿导线流向正极,质子交换膜只能氢离子通过,据此分析解答。
【详解】A.若用一氧化碳、甲烷代替图中氢气和氧气(空气),由于只有还原剂(燃料)没有氧化剂(助燃剂),故不能形成燃料电池,A错误;
B.原电池内氢离子向正极移动,B电极电极反应为:O2+4H++4e-=2H2O,B正确;
C.用该电池作为精炼铜的电源时,粗铜做阳极与电源正极相连,A为负极,C错误;
D.由于电子所带电荷与质子所带电荷相同,电性相反,所以当外电路转移0.1mol电子时,通过质子交换膜的氢离子数目0.1NA,D错误;
故合理选项是B。
【点睛】本题考查了原电池原理的知识,包括电极反应、电极正负的判断、电子守恒和质子交换膜的理解应用,掌握基础是解题关键,题目难度中等。
