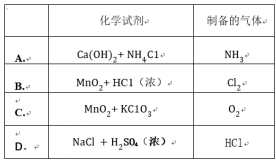
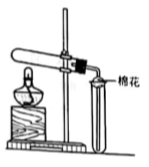
Ⅰ、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度盐酸,其操作可分为如下几步:
Ⅰ、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入用待测液润洗过的锥形瓶中,并加入3滴甲基橙溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号)________。
(2) 用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_______________。
(4)判断到达滴定终点的现象是:锥形瓶中溶液_________________________。
(5)下列操作会引起实验结果偏大的是:______(填编号)
A.滴定终点时,有一滴标准液悬挂在滴定管尖嘴处
B.观察计数时,滴定前俯视,滴定后仰视
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
E.滴定时振荡锥形瓶有溶液飞溅出去
F.配制标准NaOH溶液定容时仰视观察刻度线
Ⅱ.(6)为了检验某残留物中铁元素的含量,先将残留物预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,写出滴定过程中反应的离子方程式:________________________________________。KMnO4应装在___________滴定管中(填“酸式”或“碱式”)滴定前是否要滴加指示剂?___(填“是”或“否”),滴定终点的判断方法:_____________________________。
(7)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜加入______________调至溶液pH=4,使Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________________。[Fe(OH)3的Ksp=2.6×10-39]
答案
①④ 乙 锥形瓶内溶液颜色的变化 由红色变为橙色,且半分钟内不变色 ABF 5Fe2++8H++MnO4-=5Fe3++Mn2++4H2O 酸式 否 滴最后一滴酸性高锰酸钾溶液紫色不褪去,且30 s不变色 CuO (或Cu(OH)2或CuCO3或 Cu2(OH)2CO3) 2.6×10-9mol/L