碳、及其化合物在生产中有重要应用。
(1)设反应①Fe(s) + CO2(g)![]() FeO(s) +CO(g) △H=Q1平衡常数为K1
FeO(s) +CO(g) △H=Q1平衡常数为K1
②Fe(s) +H2O(g)![]() FeO(s) + H2(g) △H= Q2 平衡常数为K2
FeO(s) + H2(g) △H= Q2 平衡常数为K2
不同温度下,K1、K2 的值如下表
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
现有反应③H2(g) +CO2(g)![]() cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
(2)已知CO2 催化加氢合成乙醇的反应原理为:
2CO2(g) +6H2(g)![]() C2H5OH(g) + 3H2O( g) △H<O
C2H5OH(g) + 3H2O( g) △H<O

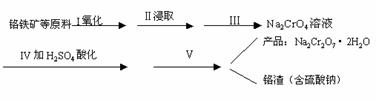
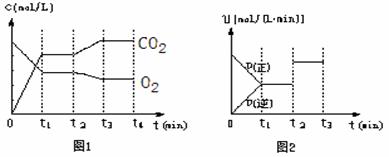
①图1、图2 分别是CO2 的平衡转化率随压强及温度的变化关系,已知m 为起始时的投料比,即m=n(H2)/n(CO2),图1中投料比相同,温度从高到低的顺序为__________,图2 中m1、m2、m3从大到小的顺序为_________。
②图3 表示在总压为5MPa的恒压条件下,且m=3 时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质为_________(填化学式),T4温度时,该反应的平衡常数Kp=___________。(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)
答案
(1)Q3=Q1-Q2(2分);吸(2 分)
(2)T3>T2>T1(2分) ;m1 >m2 >m3(2分);C2H5OH(2 分);0.243(2 分)


 ,
, ,所以
,所以