化学与科学、技术、社会、环境密切相关。下列有关说法中正确的是
A. “绿水青山就是金山银山”,矿物燃料的脱硫脱硝,可以减少SO2、NO2 的排放
B.2017 年11月5 日,发射北斗三号全球导航卫星计算机的芯片材料是高纯度二氧化硅
C.为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.2M +N=2P+2Q,2P+M=Q(M、N 为原料,Q为期望产品),不符合绿色化学的理念
A
研究化学反应原理对于生产、生活及环境保护具有重要意义。请回答下列问题:
(1)常温下,物质的量浓度均为0.1mol/L 的四种溶液①NH4NO3②CH3COONa③(NH4)2SO4④Na2CO3,pH 从大到小排列顺序为___________(填序号)。
(2)常温下,向20 mL0.2mol/LH2A溶液中滴加0.2 mol/LNaOH溶液。有关微粒物质的量变化如下图所示。
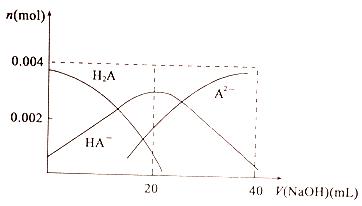
则当v(NaOH)=20 mL时,溶液中离子浓度大小关系:_________,水的电离程度比纯水_________ (填“大”、“小”或“相等”)。
(3)含有Cr2O72-的废水毒性较大,某工厂废水中含5.0×10-3mol/L 的Cr2O72-。为了使废水的排放达标,进行如下处理: ![]()
①该废水中加入绿矾(FeSO4·7H2O)和H+,发生反应的离子方程式为____________。
②若处理后的废水中残留的c(Fe2+)=2.0×10-13mol/L,则残留的Cr3+的浓度为______。
(已知:Ksp[Fe(OH)3 ]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
(4)利用“Na-CO2”电池将CO2 变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na + 3CO2![]() Na2CO3+C。放电充电时该电池“吸入”CO2,其工作原理如图所示:
Na2CO3+C。放电充电时该电池“吸入”CO2,其工作原理如图所示:
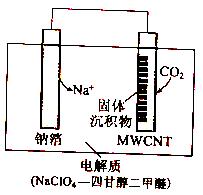
①放电时,正极的电极反应式为_________________。
②若生成的Na2CO3 和C 全部沉积在电极表面,当转移0.2mole- 时,两极的质量差为_____g。
(1) ④>②>①>③(2分)
(2)c(Na+)>c(HA-)>c(H+) >c(A2-)>c(OH-)(2分) ;小(2分)
(3) ①Cr2O72- +6Fe2++14H+=2Cr3+ +6Fe3+ +7H2O(2 分);②3.0×10-6mol/L (2分)
(4) ①3CO2 +4Na++4e-=2Na2CO3 +C(2 分);②15.8(2 分)
碳、及其化合物在生产中有重要应用。
(1)设反应①Fe(s) + CO2(g)![]() FeO(s) +CO(g) △H=Q1平衡常数为K1
FeO(s) +CO(g) △H=Q1平衡常数为K1
②Fe(s) +H2O(g)![]() FeO(s) + H2(g) △H= Q2 平衡常数为K2
FeO(s) + H2(g) △H= Q2 平衡常数为K2
不同温度下,K1、K2 的值如下表
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
现有反应③H2(g) +CO2(g)![]() cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
cCO(g) +H2O(g) △H=Q3,结合上表数据,根据反应①、②推导出推导出Q1、Q2、Q3 的关系式Q3=______________,反应③是________(填“放”或“吸”)热反应。
(2)已知CO2 催化加氢合成乙醇的反应原理为:
2CO2(g) +6H2(g)![]() C2H5OH(g) + 3H2O( g) △H<O
C2H5OH(g) + 3H2O( g) △H<O

①图1、图2 分别是CO2 的平衡转化率随压强及温度的变化关系,已知m 为起始时的投料比,即m=n(H2)/n(CO2),图1中投料比相同,温度从高到低的顺序为__________,图2 中m1、m2、m3从大到小的顺序为_________。
②图3 表示在总压为5MPa的恒压条件下,且m=3 时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质为_________(填化学式),T4温度时,该反应的平衡常数Kp=___________。(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)
(1)Q3=Q1-Q2(2分);吸(2 分)
(2)T3>T2>T1(2分) ;m1 >m2 >m3(2分);C2H5OH(2 分);0.243(2 分)
三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]· 3H2O)能溶于水,难溶于乙醇,该配合物对光敏感,光照下即发生分解。可用如下流程来制备。根据题意完成下列各题:
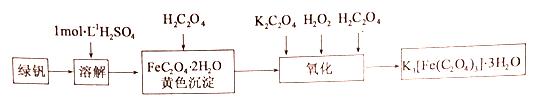
(1)溶解时加稀硫酸的作用是____________。
(2)向溶解液加人一定量的草酸后,加热煮沸,形成黄色沉淀,过滤,先涤。
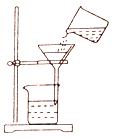
①如右图是过滤装置图请指出图中两处明显错误,一处是____________,另一处是漏斗的下尖端没有紧靠接受的烧杯。
②如何确定沉淀已经洗涤干净_________________。
(3)氧化过程中除不断搅拌外,维持温度在40C左右,原因是_________________。
(4)写出氧化生成三草酸合铁(Ⅲ)酸钾的离子方程式_________________。
(5)三草酸合铁(Ⅲ)酸钾晶体光照下即可分解生成两种草酸盐、CO2 等。写出该分解反应的化学方程式_________________。
(1)抑制Fe2+的水解(2分)
(2) ①未使用玻璃棒引流(2 分)
②取最后的洗涤液,向其中滴加盐酸酸化的氯化钡溶液,不产生白色沉淀,则已洗涤干净。(2分)
(3)温度太低反应速率慢,温度高过氧化氢会分解(2 分)
(4)2FeC2O4·2H2O+ H2O2+H2C2O4 +3C2O42-=2[ Fe(C2O4)3 ]3- +6H2O(2 分)
(5)2K3[Fe(C2O4)3]· 3H2O![]() 3K2CO4 +2FeC2O4+2CO2↑+6H2O(2 分)
3K2CO4 +2FeC2O4+2CO2↑+6H2O(2 分)
下列有关化学用语表示正确的是
A.四氯化碳分子的球棍模型: ![]() B.氢硫酸的电离:H2S
B.氢硫酸的电离:H2S![]() 2H++S2-
2H++S2-
C.氯化按的电子式: ![]() D.含78 个中子的碘原子
D.含78 个中子的碘原子![]()
D
本卷还有15题,登录并加入会员即可免费使用哦~

该作品由: 用户徐丹鸿分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。