某校化学兴趣小组为探究二氧化氮的氧化性和还原性,设计了如下装置图:
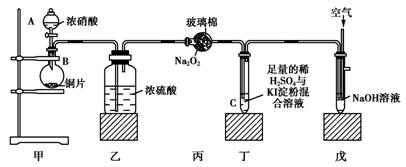
已知:2NO2+2NaOH===NaNO2+NaNO3+H2O
NO2+NO+2NaOH===2NaNO2+H2O
请回答下列问题:
(1)盛放浓硝酸的装置的名称是 ______________________________________。
(2)装置乙的作用是_______________________________________。
(3)装置丙中的实验现象为淡黄色固体变为白色,其反应为Na2O2+2NO2===2NaNO3,该实验证明
NO2具有____________________性。
(4)装置丁可证明NO2具有氧化性,其实验现象为______________,反应的化学方程式为
________________________________________________________________________。
(5)装置戊中通入空气的目的是____________________________________________。
(6)Cu(NO3)2稀溶液呈蓝色,某同学认为装置甲的B中反应后所得溶液呈绿色是由生成的红棕色NO2
溶解于溶液中引起的,请设计一个简单的实验验证其正确性:
________________________________________________________________________。
答案
答案: (1)分液漏斗
(2)除去生成的NO2中含有的水蒸气 (3)还原
(4)溶液变蓝 NO2+2KI+H2SO4===K2SO4+I2+NO+H2O
(5)将NO转化为NO2,被NaOH溶液吸收,防止污染环境
(6)将绿色溶液加水稀释,得到蓝色溶液[或往显蓝色的Cu(NO3)2溶液中通入NO2,合理即可]


