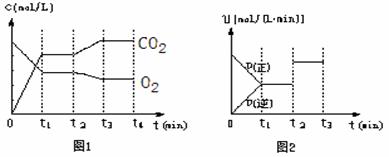
在一条件下,可逆反应2A(气)+B(气)![]() nC(固)+D(气)达平衡。若维持温度不变,增大强压,测得混合气体的平均相对分子质量不变,则下列判断正确的是( )
nC(固)+D(气)达平衡。若维持温度不变,增大强压,测得混合气体的平均相对分子质量不变,则下列判断正确的是( )
(A)其它条件不变,增大压强,平衡不发生移动
(B)其它条件不变,增大压强,混合气体的总质量不变
(C)该反应式中n值一定为2
(D)原混合气中A与B的物质的量之比为2:1,且![]() (其中M表示物质的摩尔质量)
(其中M表示物质的摩尔质量)
答案
D[分析化学方程式可得出,每有2molA、1molB转化为产物,体系中气体的物质的量就要减小2mol,气体的总质量就要减小nM(C)g或“2M(A)+M(B)”,相当于少了一种相对分子质量为![]() 或
或![]() 的气体物质]。
的气体物质]。


 ,
, ,所以
,所以