绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
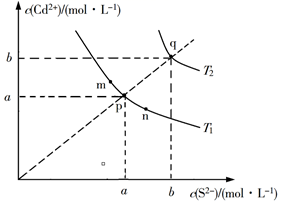
A.图中a和b分别为T1、T2温度下CdS在水中的物质的量浓度
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
B
【详解】
A. CdS在水中存在沉淀溶解平衡:CdS(s)![]() Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),在饱和溶液中,c(Cd2+)= c(S2-),结合图象可以看出,图中a和b分别表示T1和T2温度下CdS的物质的量浓度,A项正确;
Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),在饱和溶液中,c(Cd2+)= c(S2-),结合图象可以看出,图中a和b分别表示T1和T2温度下CdS的物质的量浓度,A项正确;
B. CdS的沉淀溶解平衡中的溶度积受温度影响,m、n和p点均在温度为T1条件下所测的对应离子浓度,则其溶度积相同,B项错误;
C. m点达到沉淀溶解平衡,向其中加入硫化钠后,平衡向逆反应方向移动,c(Cd2+)减小,c(S2-)增大,溶液组成由m沿mnp向p方向移动,C项正确;
D. 从图象中可以看出,随着温度的升高,离子浓度增大,说明CdS(s)![]() Cd2+(aq)+S2-(aq)为吸热反应,则温度降低时,q点对应饱和溶液的溶解度下降,溶液中的c(Cd2+)与c(S2-)同时减小,会沿qp线向p点方向移动,D项正确;
Cd2+(aq)+S2-(aq)为吸热反应,则温度降低时,q点对应饱和溶液的溶解度下降,溶液中的c(Cd2+)与c(S2-)同时减小,会沿qp线向p点方向移动,D项正确;
答案选B。
某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )
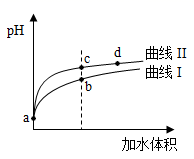
A.曲线Ⅰ代表![]() 溶液
溶液
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中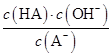 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
C
【分析】
电离常数HNO2大于CH3COOH,酸性HNO2大于CH3COOH;
A、由图可知,稀释相同的倍数,Ⅱ的变化大,则Ⅱ的酸性比I的酸性强,溶液中氢离子浓度越大,酸性越强;
B、酸抑制水电离,b点pH小,酸性强,对水电离抑制程度大;
C、kw为水的离子积常数,k(HNO2)为HNO2的电离常数,只与温度有关,温度不变,则不变;
D、体积和pH均相同的HNO2和CH3COOH溶液,c(CH3COOH)>c(HNO2)。
【详解】
A、由图可知,稀释相同的倍数,Ⅱ的变化大,则Ⅱ的酸性比I的酸性强,Ⅱ代表HNO2,I代表CH3COOH,故A错误;
B、酸抑制水电离,b点pH小,酸性强,对水电离抑制程度大,故B错误;
C、Ⅱ代表HNO2,![]() ,kw为水的离子积常数,k(HNO2)为HNO2的电离常数,这些常数只与温度有关,温度不变,则不变,故C正确;
,kw为水的离子积常数,k(HNO2)为HNO2的电离常数,这些常数只与温度有关,温度不变,则不变,故C正确;
D、体积和pH均相同的HNO2和CH3COOH溶液,c(CH3COOH)>c(HNO2),分别滴加同浓度的NaOH溶液至恰好中和,CH3COOH消耗的氢氧化钠溶液体积多,HNO2消耗的NaOH少,故D错误;
故选C。
【点睛】
本题考查酸的稀释及图象,明确强酸在稀释时pH变化程度大及酸的浓度与氢离子的浓度的关系是解答本题的关键,难点C,要将已知的c(HNO2)c(OH-)/c(NO2-)分子和分值母同乘以c(H+),变成与kw为水的离子积常数和k(HNO2)为HNO2的电离常数相关的量,再判断。
改变0.1![]() 二元弱酸
二元弱酸![]() 溶液的pH,溶液中的
溶液的pH,溶液中的![]() 、
、![]() 、
、![]() 的物质的量分数
的物质的量分数![]() 随pH的变化如图所示(已知
随pH的变化如图所示(已知![]() )。
)。

下列叙述错误的是
A.pH=1.2时,![]()
B.![]()
C.pH=2.7时,![]()
D.pH=4.2时,![]()
D
【解析】
A、根据图像,pH=1.2时,H2A和HA-相交,则有c(H2A)=c(HA-),故A说法正确;B、pH=4.2时,c(A2-)=c(HA-),根据第二步电离HA-![]() H++A2-,得出:K2(H2A)=c(H+)×c(A2-)/c(HA-)= c(H+)=10-4.2,故B说法正确;C、根据图像,pH=2.7时,H2A和A2-相交,则有c(H2A)=c(A2-),故C说法正确;D、根据pH=4.2时,c(HA-)=c(A2-),且物质的量分数约为0.48,而c(H+)=10-4.2,可知c(HA-)=c(A2-)>c(H+),故D说法错误。
H++A2-,得出:K2(H2A)=c(H+)×c(A2-)/c(HA-)= c(H+)=10-4.2,故B说法正确;C、根据图像,pH=2.7时,H2A和A2-相交,则有c(H2A)=c(A2-),故C说法正确;D、根据pH=4.2时,c(HA-)=c(A2-),且物质的量分数约为0.48,而c(H+)=10-4.2,可知c(HA-)=c(A2-)>c(H+),故D说法错误。
根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
| B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
| C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
| D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A.A B.B C.C D.D
B
【解析】
A项,苯酚的酸性弱于碳酸;
B项,CCl4将I2从碘水中萃取出来,I2在CCl4中的溶解度大于在水中的溶解度;
C项,Fe从CuSO4溶液中置换出Cu,Cu2+的氧化性强于Fe2+;
D项,向NaCl、NaI的混合液中加入AgNO3溶液产生黄色沉淀,NaCl、NaI的浓度未知,不能说明AgCl、AgI溶度积的大小。
【详解】
A项,向苯酚浊液中加入Na2CO3溶液,浊液变清,发生反应![]() +Na2CO3→
+Na2CO3→![]() +NaHCO3,酸性:H2CO3
+NaHCO3,酸性:H2CO3![]()
![]()
![]() HCO3-,A项错误;
HCO3-,A项错误;
B项,向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色,说明CCl4将I2从碘水中萃取出来,I2在CCl4中的溶解度大于在水中的溶解度,B项正确;
C项,向CuSO4溶液中加入铁粉,有红色固体析出,发生的反应为Fe+Cu2+=Fe2++Cu,根据同一反应中氧化性:氧化剂![]() 氧化产物,氧化性Cu2+
氧化产物,氧化性Cu2+![]() Fe2+,C项错误;
Fe2+,C项错误;
D项,向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成,说明先达到AgI的溶度积,但由于NaCl、NaI的浓度未知,不能说明AgCl、AgI溶度积的大小,D项错误;
答案选B。
【点睛】
本题考查苯酚与碳酸酸性强弱的探究、萃取的原理、氧化性强弱的判断、沉淀的生成。易错选D项,产生错误的原因是:忽视NaCl、NaI的浓度未知,思维不严谨。
![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol 的![]() 中,含有
中,含有![]() 个中子
个中子
B.pH=1的H3PO4溶液中,含有![]() 个
个![]()
C.2.24L(标准状况)苯在O2中完全燃烧,得到![]() 个CO2分子
个CO2分子
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加![]() 个P-Cl键
个P-Cl键
A
【解析】
A.11B中含有6个中子,0.1mol 11B含有6NA个中子,A正确;
B.溶液体积未定,不能计算氢离子个数,B错误;
C.标准状况下苯不是气体,不能利用气体摩尔体积计算22.4L苯的物质的量,则无法判断其完全燃烧产生的CO2分子数目,C错误;
D.PCl3与Cl2反应生成PCl5的反应是可逆反应,反应物不可能完全转化为生成物,则所1molPCl3与1molCl2反应生成的PCl5小于1mol,增加的P-Cl键的数目小于2NA个,D错误;答案选A。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户乐乐乐乐乐乐分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。