化学与生产、生活密切相关。下列说法正确的是( )
A. 生物柴油的成分为液态烃的混合物
B. 大量生产和使用活性炭防PM2.5口罩应对雾霾属于“绿色化学”范畴
C. 聚乙烯、油脂和淀粉均属于有机高分子化合物
D. HgCl2可用作防腐剂和杀菌剂,是因为它能使蛋白质发生变性
【答案】D
【解析】
【详解】A. 生物柴油是指由动植物油脂(脂肪酸甘油三酯)与醇(甲醇或乙醇)经酯交换反应得到的脂肪酸单烷基酯,最典型的是脂肪酸甲酯,不是烃类,A错误;
B. 绿色化学又称环境无害化学、环境友好化学、清洁化学,即减少或消除危险物质的使用和产生的化学品和过程的设计,因此大量生产和使用活性炭防PM2.5口罩应对雾霾不属于“绿色化学”范畴,B错误;
C. 聚乙烯和淀粉均属于有机高分子化合物,油脂是高级脂肪酸和甘油形成的酯类,不是高分子化合物,C错误;
D. HgCl2可用作防腐剂和杀菌剂,是因为它是重金属盐,能使蛋白质发生变性,D正确;
答案选D。
最近科学家发现使用钾和铜的微小尖峰可将二氧化碳和水转变为乙醇。下列有关化学用语表示正确的是 ( )
A. 二氧化碳的比例模型:![]() B. 中子数为34,质子数为29的铜原子:6334
B. 中子数为34,质子数为29的铜原子:6334
C. 钾原子的结构示意图: D. 乙醇的结构简式:CH3OCH3
D. 乙醇的结构简式:CH3OCH3
【答案】C
【解析】
【详解】A、CO2结构式为O=C=O,中间球为碳原子,根据原子半径大小规律,C的原子半径大于O的原子半径,故A错误;
B、根据原子构成,左上角为质量数,左下角为质子数,即该核素的表示形式为6329Cu,故B错误;
C、钾原子位于第四周期IA族,19号元素,原子结构示意图为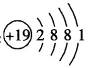 ,故C正确;
,故C正确;
D、乙醇中含有羟基,结构简式为CH3CH2OH或C2H5OH,故D错误;
NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 1L0.1mol/L的氨水中含有0.1NA个OH-
B. 常温下,在18g D2O中含有NA个氧原子
C. 常温下,7.8 g苯中所含C—H数为0.6NA
D. 标准状况下,11.2L乙烯含有非极性共价键数目为3NA
【答案】C
【解析】
【详解】A. 一水合氨是弱电解质,存在电离平衡,1L0.1mol/L的氨水中含有OH-的个数小于0.1NA个,A错误;
B. 常温下,18g D2O的物质的量是18g÷20g/mol=0.9mol,其中含有0.9NA个氧原子,B错误;
C. 常温下,7.8 g苯![]() 物质的量是7.8g÷78g/mol=0.1mol,其中所含C—H数为0.6NA,C正确;
物质的量是7.8g÷78g/mol=0.1mol,其中所含C—H数为0.6NA,C正确;
D. 标准状况下,11.2L乙烯的物质的量是11.2L÷22.4L/mol=0.5mol,含有非极性共价键数目为NA,D错误;
答案选C。
【点睛】选项D是解答的易错点,注意乙烯的结构特点,乙烯分子中含有4个碳氢单键和1个碳碳双键。其中碳氢单键是极性键,碳碳双键是非极性键。
如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1。下列叙述不正确的是( )
| R | M | X | |
| Y | Z |
A. R、Y、Z的最高价氧化物对应的水化物的酸性依次增强
B. X和Z的简单氢化物的热稳定性和还原性均依次减弱
C. R、M和氢三种元素形成的阴离子有2种以上
D. RY2分子中每个原子的最外层均为8电子稳定结构
【答案】B
【解析】
【分析】
Z原子的电子层数为n,最外层电子数为2n+1,根据元素在周期表中的相对位置可知Z位于第三周期,因此n=3,则Z是Cl,所以Y是S,X是F,M是O,R是C,结合元素周期律分析解答。
【详解】根据以上分析可知X是F,Y是S,Z是Cl,M是O,R是C,则:
A. R、Y、Z的非金属性逐渐增强,则最高价氧化物对应的水化物的酸性依次增强,A正确;
B. 非金属性O>S,因此X和Z的简单氢化物的热稳定性逐渐减弱,但还原性逐渐增强,B错误;
C. R、M和氢三种元素形成的阴离子有2种以上,例如碳酸氢根、醋酸根、草酸氢根离子等,C正确;
D. CS2分子中每个原子的最外层均为8电子稳定结构,D正确;
答案选B。
下列每组物质中含有的化学键类型相同化合物的是( )
A. NaCl、HCl、NaOH B. Na2S、H2O2、H2O
C. Cl2、H2SO4、SO2 D. HBr、 CO2、SiO2
【答案】D
【解析】
【分析】
一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。含有离子键的化合物是离子化合物,全部由共价键形成的化合物是共价化合物,据此解答。
【详解】A. NaCl是含有离子键的离子化合物,HCl是含有共价键的共价化合物,NaOH是含有离子键和共价键的离子化合物,A不选;
B. Na2S是含有离子键的离子化合物,H2O2是含有极性键和非极性键的共价化合物,H2O是含有极性键的共价化合物,B不选;
C. Cl2是含有非极性键的单质,H2SO4和SO2均是含有共价键的共价化合物,C不选;
D. HBr、CO2、SiO2均是含有极性键的共价化合物,D选;
答案选D。
【点睛】明确离子键和共价键的形成条件以及化学键和化合物类型的关系是解答的关键,需要注意的是金属和非金属之间不一定形成离子键,例如氯化铝中不存在离子键。另外离子化合物可以含有共价键,但共价化合物中一定不能含有离子键。
本卷还有21题,登录并加入会员即可免费使用哦~

该作品由: 用户王啸天分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。