下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ/mol
2NH3(g) ΔH=-38.6kJ/mol
C.吸热反应的发生都需要加热,放热反应在常温下一定容易发生
D.表示中和热的离子方程式为H+(aq) +OH-(aq)![]() H2O(l) ΔH=-57.3kJ/mol
H2O(l) ΔH=-57.3kJ/mol
【答案】D

考点:化学反应中的能量变化
已知下列热化学反应方程式:
①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g);△H=-26.7 kJ/mol
②2Fe3O4(s)+ CO2(g)═3Fe2O3(s)+ CO(g);△H=+50.75 kJ/mol
③3/2FeO(s)+1/2CO2(g)═1/2Fe3O4(s)+1/2CO(g);△H=+18.25 kJ/mol
则反应Fe(s)+CO2 (g)= FeO(s)+CO(g)的焓变为
A.+7.28 kJ/mol B.-7.28 kJ/mol C.+43.65 kJ/mol D.-43.68 kJ/mol
【答案】B
【解析】
试题分析:由盖斯定律可知,(①×3+②+③×4)÷6,得到反应FeO(s)+CO(g)=Fc(s)+CO2(g),
△H==+7.28kJ/mol,则反应Fe(s)+CO2 (g)= FeO(s)+CO(g)的焓变为-7.28 kJ/mol,故选B。
考点:考查用盖斯定律进行有关反应热的计算
【名师点晴】本题考查学生利用盖斯定律计算反应热,熟悉已知反应与目标反应的关系是解答本题的关键。应用盖斯定律进行简单计算的基本方法是参照新的热化学方程式(目标热化学方程式),结合原热化学方程式(一般2~3个)进行合理“变形”,如热化学方程式颠倒、乘除以某一个数,然后将它们相加、减,得到目标热化学方程式,求出目标热化学方程式的ΔH与原热化学方程式之间ΔH的换算关系。
下图甲和乙是双液原电池装置。由图可判断下列说法正确的是
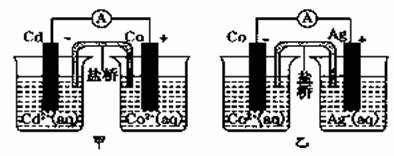
A.甲图电池反应的离子方程式为Co(s)+Cd2+(aq) = Cd(s)+Co2+(aq)
B.由乙图可知,2Ag(s)+ Co2+(aq) = Co(s) +2Ag+(aq)反应能够发生
C.盐挢的作用是形成闭合回路,并使两边溶液保持电中性,电池工作时盐桥中的阳离子移向正极
D.乙图中,当有lmol电子通过外电路时,正极有54克Ag析出
【答案】C

考点:原电池的原理
有A、B、C、D四种金属,进行如下实验:①将A与B浸在稀硫酸中用导线相连,A逐渐溶解,B上有气泡逸出;②将A、D分别投入等浓度盐酸中,D比A反应剧烈;③将B浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C
C.D>B>A>C D.B>A>D>C
【答案】B
【解析】
【答案】B

考点:考查金属活泼性强弱的判断
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意图如下,下列说法中正确的是

A.b极为电池的负极
B.电池工作时电子在内电路中由a极经溶液到b极
C.电池负极的电极反应为:C2H5OH+3H2O-12e-==2CO2+12H+
D.电池工作时,1mol乙醇被氧化时有6mol电子转移
【答案】C
【解析】
试题分析:A.在燃料电池中,燃料乙醇在负极发生失电子的反应,氧气是在正极上发生得电子的反应,则a为负极,故A错误;B.电池工作时,电子在外电路中由a极经溶液到b极,内电路中是电解质溶液中的阴阳离子定向移动,故B错误;C.在燃料电池中,正极上是氧气得电子的还原反应,在酸性电解质环境下,正极的电极反应为:4H++O2+4e-=2H2O,燃料乙醇在负极发生失电子的氧化反应,负极的电极反应为:C2H5OH+3H2O-12e-==2CO2+12H+,故C正确;D.根据电池反应:C2H5OH+3O2=2CO2+3H2O,则1mol乙醇被氧化失去12mol电子,所以1mol乙醇被氧化电路中转移12NA的电子,故D错误;答案为C。
考点:考查原电池原理。
本卷还有18题,登录并加入会员即可免费使用哦~

该作品由: 用户唐迪生分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。