化学与人们的日常生活密切相关,下列叙述正确的是( )
A.水玻璃可用于生产黏合剂和防火剂
B.纤维素、油脂是天然有机高分子化合物
C.白菜上洒少许福尔马林,既保鲜又消毒
D.棉、麻、合成纤维完全燃烧都只生成CO2和H2O
【考点】含硅矿物及材料的应用;常见的食品添加剂的组成、性质和作用;有机高分子化合物的结构和性质.
【分析】A.根据水玻璃的性质分析;
B.油脂是小分子有机化合物;
C.甲醛有毒,不能用来保鲜食品;
D.棉、麻属于纤维素,羊毛属于蛋白质,合成纤维是以小分子的有机化合物为原料,经加聚反应或缩聚反应合成的线型有机高分子化合物,分子中出C、H元素外,还含有其它元素,如N元素等.
【解答】解:A.水玻璃是硅酸钠的水溶液,硅酸钠具有黏性,所以可作粘合剂;涂有硅酸钠溶液的木条加热时,水分蒸发后不易燃烧,所以可作防火剂,故A正确;
B.纤维素是天然有机高分子化合物,油脂不是高分子化合物,故B错误;
C.甲醛有毒,能破坏蛋白质的结构,对人体有害,不能用来保鲜食品,故C错误;
D.棉、麻属于纤维素,含有C、H两种元素,完全燃烧只生成CO2和H2O;羊毛属于蛋白质,含有C、H、O、N等元素,完全燃烧除生成CO2和H2O,还有其它物质生成;合成纤维是以小分子的有机化合物为原料,经加聚反应或缩聚反应合成的线型有机高分子化合物,分子中出C、H元素外,还含有其它元素,如N元素等,完全燃烧除生成CO2和H2O,还有其它物质生成,故D错误;
故选:A.
【点评】本题考查了生活中常见物质的用途,熟悉硅酸钠、甲醛、合成纤维的性质是解题关键,注意高分子化合物的判断,题目难度不大.
下列叙述正确的是( )
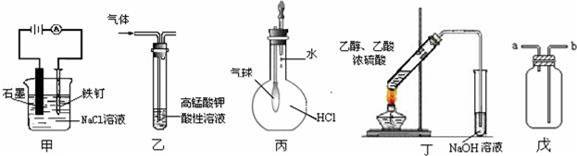

①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体.
A.①⑤ B.②④ C.③④ D.③⑤
【考点】化学实验方案的评价.
【分析】①金属做电解池的阳极时,更易被腐蚀;
②高锰酸钾具有氧化性,可以将乙烯以及乙炔氧化为二氧化碳;
③氯化氢极易溶于水,根据大气压强原理来分析;
④乙酸乙酯可以用饱和碳酸钠来吸收;
⑤装置可以收集气体,当集气瓶来用,但是要注意导管的连接情况.
【解答】解:①在装置中,金属Fe做电解池的阳极,电极本身失电子,更易生锈,故①错误;
②高锰酸钾具有氧化性,可以将乙烯以及乙炔氧化为二氧化碳,不能用装置乙可除去乙烯中混有的乙炔,故②错误;
③氯化氢极易溶于水,挤压胶头滴管,则集气瓶中压强减小,所以气球鼓起来,可以使用该装置验证HCl气体在水中的溶解性,故③正确;
④乙酸乙酯可以用饱和碳酸钠来吸收,不能用氢氧化钠,乙酸乙酯在氢氧化钠中水解,故④错误;
⑤装置可以收集气体,当集气瓶来用,导管长进短出时,可以收集密度大于空气的气体,如:CO2、Cl2、HCl、NO2等气体,如果导管短进长出,则可以收集密度小于空气的气体,如氢气,故⑤正确.
故选D.
【点评】本题是一道化学实验知识的综合题目,实验为载体考查基础知识,以要求学生熟记教材知识,灵活应用.
有机物C4H8Cl2的结构中只含有一个甲基的同分异构体有几种(不考虑立体异构)( )
A.3 B.4 C.7 D.8
【考点】同分异构现象和同分异构体.
【分析】二氯代物的同分异构体可以采用“定一移二”法解题,先找出所有的同分异构体,再找出只含一个“﹣CH3”的.
【解答】解:C4H8Cl2的同分异构体可以采取“定一移二”法
 ,由图可知C4H8Cl2共有9种同分异构体,其中图1中另一氯在1、2、3三个碳原子上,分子中都只有1个甲基,图2中另一氯在1、2号碳上,分子中都含2个甲基,图3中另一氯在3号碳上,分子中只含1个甲基,所以分子中含1个甲基的同分异构体有共4种;
,由图可知C4H8Cl2共有9种同分异构体,其中图1中另一氯在1、2、3三个碳原子上,分子中都只有1个甲基,图2中另一氯在1、2号碳上,分子中都含2个甲基,图3中另一氯在3号碳上,分子中只含1个甲基,所以分子中含1个甲基的同分异构体有共4种;
故选B.
【点评】本题考查有机物的同分异构体的书写,难度不大,注意二氯代物的同分异构体可以采用“定一移二”法解题.
下列叙述正确的是(NA表示阿伏伽德罗常数)( )
A.7.8g过氧化钠含有的共用电子对数为0.2NA
B.过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢得到2NA电子
C.在含有NH4+、Ba2+、Cl﹣、NO3﹣离子的溶液 加入过氧化钠以上各离子量几乎不减少
D.2H2O2(l)═2H2O(l)+O2(g);△H=﹣98.2 kJ/mol,△S=70.5 J/mol•K,该反应低温能自发进行
【考点】阿伏加德罗常数.
【专题】阿伏加德罗常数和阿伏加德罗定律.
【分析】A、7.8g过氧化钠粉含有的共用电子对数为0.1NA;
B、过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢失去2NA电子;
C、铵根离子与氢氧根离子反应生成氨水;
D、根据吉布斯自由能公式△G=△H﹣T△S分析.
【解答】解:A、7.8g过氧化钠粉末物质的量为0.1mol,含有的共用电子对数为0.1NA,故A错误;
B、过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢失去2NA电子,故B错误;
C、过氧化钠与水反应生成NaOH,铵根离子与氢氧根离子反应生成氨水,故C错误;
D、根据吉布斯自由能公式△G=△H﹣T△S,低温能自发进行,故D正确.
故选D.
【点评】本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
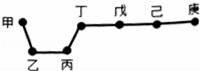

A.甲一定是金属元素
B.气态氢化物的稳定性:庚>己>戊
C.庚的最高价氧化物的水化物酸性最强
D.乙、丙、丁的最高价氧化物的水化物可以以相互反应
【考点】原子结构与元素的性质.
【分析】短周期元素甲、乙、丙、丁、戊、己、庚,戊、己分别是空气、地壳中含量最多的元素,则戊为N元素,己为O元素,所以丁、戊、己、庚为第二周期元素,则乙、丙为第三周期元素,甲不一定在丁、庚的连线上,则甲为第一周期元素,则甲为H元素,根据元素在周期表中位置关系可知,乙为Mg元素,丙为Al,丁为C元素,庚为F元素,据此答题.
【解答】解:短周期元素甲、乙、丙、丁、戊、己、庚,戊、己分别是空气、地壳中含量最多的元素,则戊为N元素,己为O元素,所以丁、戊、己、庚为第二周期元素,则乙、丙为第三周期元素,甲不一定在丁、庚的连线上,则甲为第一周期元素,则甲为H元素,根据元素在周期表中位置关系可知,乙为Mg元素,丙为Al,丁为C元素,庚为F元素.
A.根据上面的分析可知,甲为氢元素,为非金属元素,故A错误;
B.同周期自左而右非金属性增强,氢化物稳定性与元素非金属一致,故气态氢化物的稳定性HF>H2O>NH3,故B正确;
C.庚为氟元素,氟元素没有最高正价含氧酸,故C错误;
D.乙、丙、丁的最高价氧化物的水化物分别为氢氧化镁、氢氧化铝、碳酸,碳酸为弱酸,不能溶解氢氧化铝、氢氧化镁,氢氧化镁与氢氧化铝不能反应,故D错误,
故选B.
【点评】本题考查结构性质位置关系,明确元素种类是解题关键,注意元素处于不同的族及周期,侧重对基础知识的巩固.
本卷还有8题,登录并加入会员即可免费使用哦~

该作品由: 用户lily分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。