下列说法正确的是
A . HCl 的电子式为 ![]() B .乙炔的结构简式: C 2 H 2
B .乙炔的结构简式: C 2 H 2
C . CH 3 CHOHCH 3 的名称: 2- 丙醇 D .中子数为 2 的 He 原子可表示为
C
【详解】 A . HCl 是共价化合物, H 原子与 Cl 原子通过一个共价键结合,使分子中各个原子都达到稳定结构,故 HCl 的电子式为: ![]() , A 错误;
, A 错误;
B .乙炔分子式是 C 2 H 2 ,分子中 2 个 C 原子形成共价三键,每个 C 原子分别与 1 个 H 原子形成共价单键,故其的结构简式为 HC≡CH , B 错误;
C . CH 3 CHOHCH 3 分子中 -OH 与连接在第二个 C 原子,因此其名称为: 2- 丙醇, C 正确;
D .原子符号左下角为质子数,左上角为质量数,质量数等于质子数与中子数的和,则中子数为 2 的 He 原子质量数为 2+2=4 ,因此可表示为 , D 错误;
故合理选项是 C 。
下列化学用语正确的是
A .乙烯的结构式为
B .次氯酸的电子式为 ![]()
C .乙酸的比例模型为 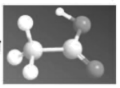
D .异戊烷的系统命名为 2- 甲基丁烷
D
【详解】 A .乙烯的分子式为 ,结构式为
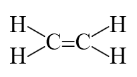 , A 错误;
, A 错误;
B .次氯酸的电子式为 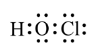 , B 错误;
, B 错误;
C .图示为乙酸的球棍模型,不是比例模型 ( 空间填充模型 ) , C 错误;
D .异戊烷的结构简式为 CH(CH 3 ) 2 CH 2 CH 3 ,系统命名为 2- 甲基丁烷, D 正确;
答案选 D 。
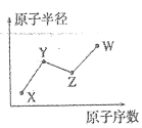
W 、 X 、 Y 、 Z 是四种常见的短周期元素,其原子半径随原子序数的变化如图所示。已知 Y 、 Z 两种元素单质是空气的主要成分, W 原子的核外电子数与 Ne 相差 1 , X 与 W 同主族。下列说法正确的是
A . W 与 Z 形成的化合物只有离子键 B . X 与 Y 形成的化合物的电子式为: ![]()
C . W 的最高价氧化物对应水化物呈碱性 D . Z 的氢化物只有 1 种
C
【分析】 Y 、 Z 两种元素单质是空气的主要成分,原子半径 Y>Z ,故 Y 为 N , Z 为 O ; W 原子的核外电子数与 Ne 相差 1 ,且原子半径 W>N ,故 W 为 Na ; X 与 W 同主族,且原子半径 X<N ,故 X 为 H 。
【详解】 A . Na 与 O 可形成 Na 2 O 2 ,含离子键和共价键, A 错误;
B .氨气的电子式中 N 原子应满足 8 电子稳定结构,电子式错误, B 错误;
C . W 的最高价氧化物对应水化物为 NaOH ,呈碱性, C 正确;
D . Z 的氢化物为 H 2 O 和 H 2 O 2 , D 错误;
故选 C 。
下列化学用语正确的是
A .硫原子的结构示意图: 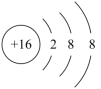
B . 的电子式为
![]()
C . 在水溶液中电离方程式:
D . KCl 形成过程: ![]()
B
【详解】 A .硫原子的核电荷数为 16 ,最外层电子数为 6 ,其原子结构示意图为  ,故 A 错误;
,故 A 错误;
B . Na 2 O 2 由 Na + 和 构成,
中 O 原子间共用 1 对电子, O 原子最外层电子数为 8 ,则 Na 2 O 2 的电子式为
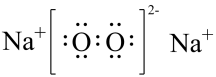 ,故 B 正确;
,故 B 正确;
C . 在水溶液中电离产生 Na + 和
,其电离方程式为
,故 C 错误;
D . KCl 为离子化合物,由 K + 和 Cl - 构成,用电子式表示其形成过程为: ![]() ,故 D 错误;
,故 D 错误;
故答案选 B 。
下列化学用语使用正确的是
A . Ca 处于基态的电子排布式为:
B .  是手性分子
是手性分子
C . 的电子式:
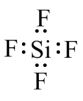
D .氧元素基态原子的电子排布图为: 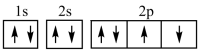
B
【详解】 A .钙元素的原子序数为 20 ,基态原子的电子排布式为 ,故 A 错误;
B .由图可知,图中有机物分子中含有的碳原子是连有 4 个不同的原子或原子团的手性碳原子,所以该分子是手性分子,故 B 正确;
C .四氟化硅是共价化合物,电子式为 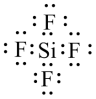 ,故 C 错误;
,故 C 错误;
D .氧元素的原子序数为 8 ,基态原子的电子排布图为  ,故 D 错误;
,故 D 错误;
故选 B 。
本卷还有30题,登录并加入会员即可免费使用哦~

该作品由: 用户111111分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。