石墨的片层与层状结构如图2-19所示:其中C—C键长为![]() ,层间距离为
,层间距离为![]() .试回答:
.试回答:
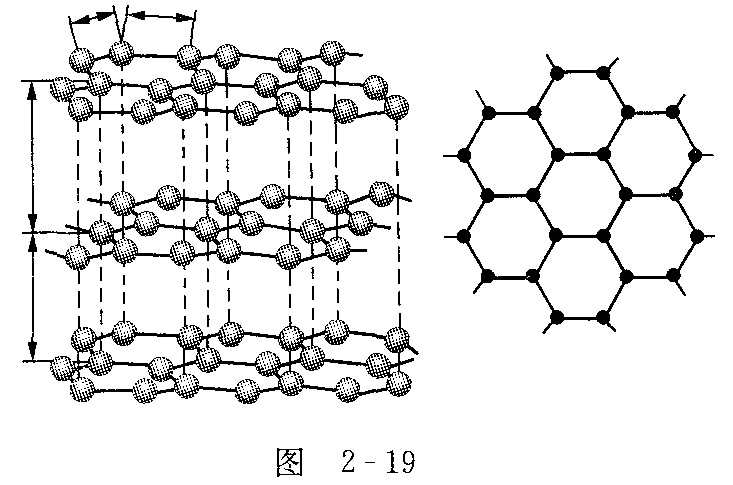
(1)片层中平均每个六元环含碳原子数为_____个;在层状结构中,平均每个六棱柱含碳原子数_____个.
(2)在片层结构中,碳原子数、C—C键数、六元环数之比为________.
(3)已知下列公式及数据:正六边形面积=![]() (a为正六边形的边长);
(a为正六边形的边长);![]() ;
;![]() ,求12g石墨的体积(保留三位有效数字).
,求12g石墨的体积(保留三位有效数字).
答案
(1)2个 2个 (2)2:3:1 (3)5.25![]() 或5.29
或5.29![]() (提示:在石墨的片层结构中,一个六元环平均拥有的碳原子数为6×1/3=2;属于每个六元环的碳碳键数为6×1/2=3.至此,应以六棱柱建立数学模型,不难看出每个六棱柱平均拥有2个碳原子.求出这个2个碳原子的质量和正六棱柱的体积,就能求出密度,已知密度便可求出12g石墨的体积)
(提示:在石墨的片层结构中,一个六元环平均拥有的碳原子数为6×1/3=2;属于每个六元环的碳碳键数为6×1/2=3.至此,应以六棱柱建立数学模型,不难看出每个六棱柱平均拥有2个碳原子.求出这个2个碳原子的质量和正六棱柱的体积,就能求出密度,已知密度便可求出12g石墨的体积)


 表示,分子用化学式表示,离子用
表示,分子用化学式表示,离子用 表示。
表示。