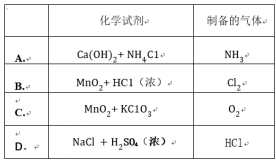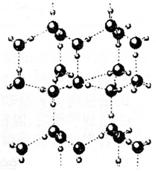
(1)1 mol冰中有___________ mol“氢键”。
(2)水分子可电离生成两种含有相同电子数的微粒,其电离方程式为_________________。
(3)用x、y、z分别表示H2O、H2S、H2Se的沸点(℃)则x、y、z的大小关系是__________。
(4)实验测得冰中氢键的作用能为18.8 kJ·mol-1,而冰的熔化热为5.0 kJ·mol-1,这说明______________________________。
答案
(1)2
(2)H2O+H2O![]() H3O++OH-
H3O++OH-
(3)x>z>y
(4)液态水中仍然存在大量氢键
解析:晶体冰中,每两个水分子间有一个氢键,平均属于每个水分子有半个,一个水分子与周围的四个水分子以氢键结合,故1 mol冰中有2 mol氢键。