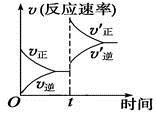
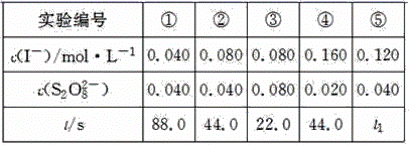
某兴趣小组设计实验探究 ,催化空气氧化
的效率。回答下列问题:
步骤 Ⅰ 制备
在通风橱中用下图装置制备 ( 加热及夹持装置省略 ) ,反应方程式:
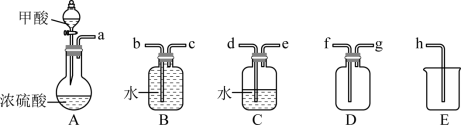
(1) 装置 A 中盛放甲酸的仪器的名称是 。
(2) 从 B 、 C 、 D 中选择合适的装置收集 ,正确的接口连接顺序为 a→_______→_______→_______→_______→h( 每空填一个接口标号 ) 。
步骤 Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
(3) 该反应的化学方程式为 。
步骤 Ⅲ 探究 催化空气氧化
的效率
将一定量 与空气混合,得到
体积分数为 1% 的气体样品。使用下图装置 ( 部分加热及夹持装置省略 ) ,调节管式炉温度至
,按一定流速通入气体样品。 ( 已知:
是白色固体,易吸水潮解:
)
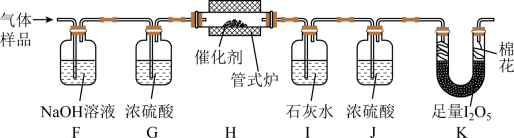
(4) 通入 ( 已折算为标况 ) 的气体样品后,继续向装置内通入一段时间氮气,最终测得 U 形管内生成了
。
① 能证明 被空气氧化的现象是 ;
② 被催化氧化的百分率为 ;
③ 若未通入氮气, ② 的结果将 ( 填 “ 偏大 ”“ 偏小 ” 或 “ 无影响 ”) 。
(5) 探究气体与催化剂接触时长对催化氧化效率的影响时,采用 方法可以缩短接触时长。
(6) 步骤 Ⅲ 装置存在的不足之处是 。
答案
(1) 分液漏斗
(2)a→d→e→c→b
(3)
(4) 石灰水变浑浊 60% 偏大
(5) 增大气体样品流速
(6) 尾气出口未加防潮装置 ( 或其他相似表述 )
【分析】在通风橱中用下图装置制备一氧化碳,用 A 装置制取一氧化碳,该气体中含有甲酸蒸气,故用水除去甲酸,再用 B 装置排水收集一氧化碳气体,排出的水用 E 中的烧杯接收。根据气体样品通过氢氧化钠吸收空气中的二氧化碳,浓硫酸吸水,一氧化碳在 H 中被氧气氧化生成二氧化碳,二氧化碳能被石灰水吸收, J 中的浓硫酸吸收气体中的水蒸气,干燥的一氧化碳和 ,进而测定生成的碘的质量,计算一氧化碳的被氧化的百分率。据此解答。
【详解】( 1 )装置 A 中盛放甲酸的仪器为分液漏斗。
( 2 )用 C 除去甲酸, B 收集一氧化碳, E 接收排出的水,故接口连接顺序为 a→d→e→c→b→h 。
( 3 )一氧化碳和银氨溶液反应生成黑色的银,同时生成碳酸铵和氨气,方程式为: 。
( 4 )一氧化碳被氧气氧化生成二氧化碳,能使澄清的石灰水变浑浊。碘的物质的量为 ,则结合方程式分析,还有 0.002mol 一氧化碳未被氧气氧化, 11.2L 气体为 0.5mol 其中一氧化碳为 0.005mol ,则被氧化的一氧化碳为 0.005-0.002=0.003mol ,则被氧化的百分率为
。如果没有通入氮气则计算的未被氧化的一氧化碳的物质的量减少,则被氧化的百分率增大。
( 5 )增大气流速率可以提高催化效率。
( 6 ): 是白色固体,易吸水潮解,但该装置出气口未加防潮装置。