锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有 和
杂质离子,可在 0~14 范围内调节
对其净化 ( 即相关离子浓度
) 。
时,
与
关系见下图 ( 碱性过强时
和
会部分溶解 ) 。下列说法正确的是
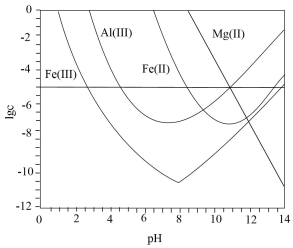
A . 可被净化的
区间最大
B .加入适量 ,可进一步提升净化程度
C .净化的先后顺序:
D .
答案
B
【详解】 A .对离子净化时,相关离子浓度 c <10 -5 mol/L ,则 lg c <-5 ,由图可知,可作净化的 pH 区间最大的是 Fe 3+ , A 错误;
B .加入适量 H 2 O 2 ,可将 Fe 2+ 氧化为 Fe 3+ ,提高净化程度, B 正确;
C .由图可知,净化的先后顺序为 , C 错误;
D .对离子净化时,相关离子浓度 c <10 -5 mol/L , lg c <-5 ,,由图可知, Fe 3+ 完全沉淀的 pH 约为 2.5 , c (H + )=10 -2.5 mol/L , c (OH - )=10 -11.5 mol/L , , Al 3+ 完全沉淀的 pH 约为 4.5 , c (H + )=10 -4.5 mol/L , c (OH - )=10 -9.5 mol/L ,
, Fe 2+ 完全沉淀的 pH 约为 8.5 , c (H + )=10 -8.5 mol/L , c (OH - )=10 -5.5 mol/L ,
,则有
, D 错误;
故选 B 。


 Ag+(aq)+Cl-(aq),加入AgNO3,平衡向沉淀方向移动,Cl-减少。
Ag+(aq)+Cl-(aq),加入AgNO3,平衡向沉淀方向移动,Cl-减少。  转变为
转变为 沉淀而除去。
沉淀而除去。 
 等作沉淀剂,使某些金属离子如
等作沉淀剂,使某些金属离子如 等生成极难溶的硫化物
等生成极难溶的硫化物
 等沉淀,也是分离、除杂常用的方法。
等沉淀,也是分离、除杂常用的方法。
 时即沉淀完全。
时即沉淀完全。  平衡就会向沉淀溶解的方向移动,使沉淀溶解。
平衡就会向沉淀溶解的方向移动,使沉淀溶解。  沉淀中加入
沉淀中加入 溶液,
溶液, 结合生成
结合生成 使
使 的溶解平衡向右移动。
的溶解平衡向右移动。 




 中加入饱和
中加入饱和 溶液使
溶液使 转化为
转化为 再将
再将 溶于盐酸。
溶于盐酸。