科学家合成了一种新的共价化合物 ( 结构如图所示 ) , X 、 Y 、 Z 、 W 为原子序数依次增大的短周期元素, W 的原子序数等于 X 与 Y 的原子序数之和。下列说法错误的是
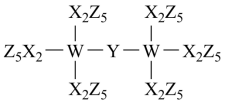
A .原子半径: B .非金属性:
C . Z 的单质具有较强的还原性 D .原子序数为 82 的元素与 W 位于同一主族
答案
C
【分析】由共价化合物的结构可知, X 、 W 形成 4 个共价键, Y 形成 2 个共价键, Z 形成 1 个共价键, X 、 Y 、 Z 、 W 是原子序数依次增大的短周期元素, W 的原子序数等于 X 与 Y 的原子序数之和,则 X 为 C 元素、 Y 为 O 元素、 Z 为 F 元素、 W 为 Si 元素。
【详解】 A .同周期元素,从左到右原子半径依次减小,则 C 、 O 、 F 的原子半径大小顺序为 C > O > F ,故 A 正确;
B .同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减弱,则 C 、 O 、 Si 的非金属性强弱顺序为 O > C > Si ,故 B 正确;
C .位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故 C 错误;
D .原子序数为 82 的元素为铅元素,与硅元素都位于元素周期表 ⅣA 族,故 D 正确;
故选 C 。
