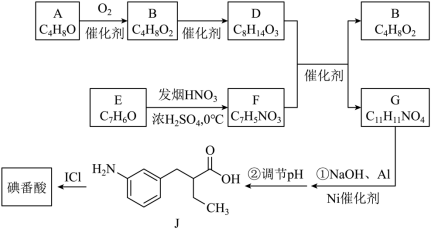
碘番酸是一种口服造影剂,用于胆部 X— 射线检查。其合成路线如下:
已知: R 1 COOH+R 2 COOH
![]() +H 2 O
+H 2 O
(1)A 可发生银镜反应, A 分子含有的官能团是 。
(2)B 无支链, B 的名称是 。 B 的一种同分异构体,其核磁共振氢谱只有一组峰,结构简式是 。
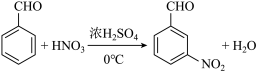
(3)E 为芳香族化合物, E→F 的化学方程式是 。
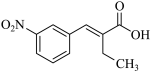
(4)G 中含有乙基, G 的结构简式是 。
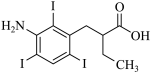
(5) 碘番酸分子中的碘位于苯环上不相邻的碳原子上。碘番酸的相对分子质量为 571 , J 的相对分子质量为 193 ,碘番酸的结构简式是 。
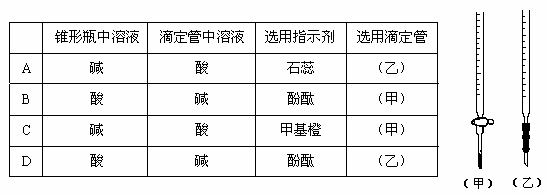
(6) 口服造影剂中碘番酸含量可用滴定分析法测定,步骤如下。
步骤一:称取 amg 口服造影剂,加入 Zn 粉、 NaOH 溶液,加热回流,将碘番酸中的碘完全转化为 I - ,冷却、洗涤、过滤,收集滤液。
步骤二:调节滤液 pH ,用 bmol∙L -1 AgNO 3 标准溶液滴定至终点,消耗 AgNO 3 溶液的体积为 cmL 。
已知口服造影剂中不含其它含碘物质。计算口服造影剂中碘番酸的质量分数 。
答案
(1) 醛基
(2) 正丁酸 ![]()
(3) 
(4) 
(5) 
(6)
【分析】本流程的目的,以 A 为原料制取碘番酸。由 A 可发生银镜反应,可确定 A 为醛,由 B 无支链,可确定 B 为 CH 3 CH 2 CH 2 COOH ,则 A 为 CH 3 CH 2 CHO ;依据题干信息,可确定 D 为 ![]() ; E 为芳香族化合物,则 E 为
; E 为芳香族化合物,则 E 为 ![]() ;由 J 的结构简式
;由 J 的结构简式 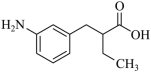 ,可确定 F 为
,可确定 F 为 ![]() 。由题给信息,要确定 G 为
。由题给信息,要确定 G 为 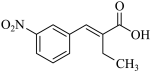 。
。
【详解】( 1 )由 A 的分子式 C 4 H 8 O 及可发生银镜反应,可确定 A 分子含有的官能团是醛基。答案为:醛基;
( 2 ) B 的分子式为 C 4 H 8 O 2 、无支链,由醛氧化生成,则 B 为 CH 3 CH 2 CH 2 COOH ,名称是正丁酸。 B 的一种同分异构体,其核磁共振氢谱只有一组峰,则表明分子中 8 个 H 原子全部构成 -CH 2 - , B 的不饱和度为 1 ,则其同分异构体应具有对称的环状结构,从而得出其结构简式是 ![]() 。答案为:正丁酸;
。答案为:正丁酸; ![]() ;
;
( 3 )由分析知, E 为 ![]() , F 为
, F 为 ![]() ,则 E→F 的化学方程式是
,则 E→F 的化学方程式是 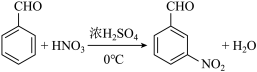 。答案为:
。答案为: 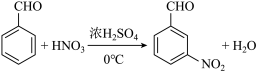 ;
;
( 4 )由分析可知, G 的结构简式是 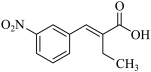 。答案为:
。答案为: 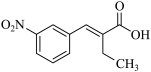 ;
;
( 5 )碘番酸的相对分子质量为 571 , J 的相对分子质量为 193 ,由相对分子质量差可确定, J 生成碘番酸时,分子中引入 3 个 I 原子,而碘番酸分子中的碘位于苯环上不相邻的碳原子上,则碘番酸的结构简式是 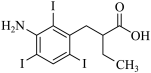 。答案为:
。答案为: 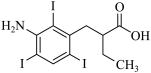 ;
;
( 6 ) 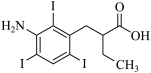 ——3AgNO 3 , n (AgNO 3 )= bmol∙L -1 ×c×10 -3 L=bc×10 -3 mol ,则口服造影剂中碘番酸的质量分数为
——3AgNO 3 , n (AgNO 3 )= bmol∙L -1 ×c×10 -3 L=bc×10 -3 mol ,则口服造影剂中碘番酸的质量分数为 =
。答案为:
。
【点睛】推断有机物时,官能团可由反应条件确定,结构可依据转化前后对应物质的结构简式确定。




 可知,
可知, 是准 确量取的体积,
是准 确量取的体积, 是标准溶液的浓度,它们均为定值,所以
是标准溶液的浓度,它们均为定值,所以 的大小取决于
的大小取决于 的大小,
的大小, 大则
大则 大,
大, 小则
小则 小。
小。