海冰是海水冻结而成的咸水冰,海水冻结时,部分来不及流走的盐分 ( 设为 NaCl) 以卤汁的形式被包围在冰晶之间,形成 “ 盐泡 ” ,若海冰的冰龄达到 1 年以上,融化后的水为淡水。其大致结构如图所示。下列叙述正确的是
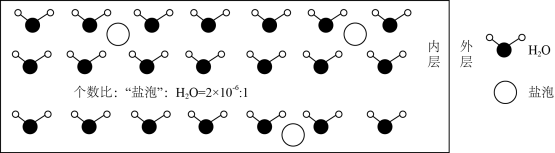
A .海冰冰龄越长, “ 盐泡 ” 越多
B .海冰内层 “ 盐泡 ” 越多,密度越小
C .每含 1mol 水的海冰内有 2×10 -6 N A 个 NaCl 分子
D .海冰内层 NaCl 的浓度约为 1.0×10 -4 mol/L( 设海冰的密度为 0.9 g/cm 3 )
答案
D
【详解】 A .若海冰的冰龄达到 1 年以上,则融化后的水为淡水,说明海冰冰龄越长,内层的 “ 盐泡 ” 越少, A 错误;
B .海冰内层 “ 盐泡 ” 越少,来不及流走的盐分越少,密度越小, B 错误;
C . NaCl 属于离子化合物,不存在 NaCl 分子, C 错误;
D .设海冰内层体积为 1L ,则冰的质量为 0.9g/cm 3 ×1000cm 3 =900g ,则 n (H 2 O)= =50mol , n (NaCl)∶ n (H 2 O)= N (NaCl)∶ N (H 2 O)=(2×10 -6 )∶1 , n (NaCl)=50mol×2×10 -6 =10 -4 mol ,则 NaCl 的浓度约为 10 -4 mol÷1L=10 -4 mol/L , D 正确;
故选 D 。
