已知 X 、 Y 、 Z 、 W 是中学化学中常见的 4 种物质 (X 、 Y 、 Z 含有相同元素 ) ,其转化关系符合下图。下列说法错误的是
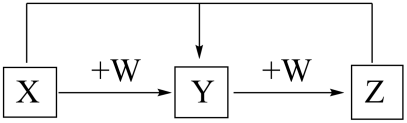
A .若 是非氧化还原反应,则 W 可能是碱溶液
B .若 是非氧化还原反应,则 W 可能是酸溶液
C .若 是氧化还原反应,则 X 可能是金属铝
D .若 是氧化还原反应,则 X 可能是非金属碳
答案
C
【详解】 A .若 Y+W→Z 是非氧化还原反应,若 W 是碱溶液, X 可以是氯化铝, W 是氢氧化钠, Y 是氢氧化铝, Z 是偏铝酸钠,氯化铝与偏铝酸钠反应生成氢氧化铝,符合转化关系,故 A 正确;
B .若 Y+W→Z 是非氧化还原反应,若 W 是酸溶液, X 可以是偏铝酸钠, W 是盐酸等, Y 是氢氧化铝, Z 是氯化铝,氯化铝与偏铝酸钠反应生成氢氧化铝,符合转化关系,故 B 正确;
C .若 Y+W→Z 是氧化还原反应,则 W 或 X 中应有可变化合价的元素,则 W 不可能是金属铝,故 C 错误;
D .若 Y+W→Z 是氧化还原反应,则 W 是非金属碳,则 X 可以是氧气, Y 是二氧化碳, Z 是一氧化碳,氧气与一氧化碳反应生成二氧化碳,符合转化关系,故 D 正确;
故选: C 。


