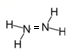
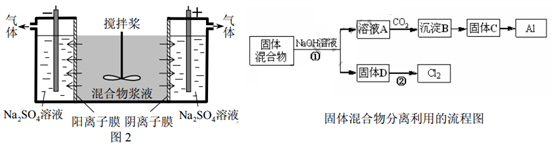
下面叙述不正确的是
A . S 2- 的结构示意图 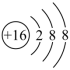 B .
B . 的电子数为 136
C .质子数为 35 、中子数为 45 的溴原子: Br D .
Ti 的中子数是 26
答案
B
【详解】 A .硫原子得到 2 个电子形成硫离子, S 2- 的结构示意图 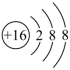 , A 正确;
, A 正确;
B .核素的表示方法为:元素符号左下角为质子数,左上角为质量数,原子中质子数 = 电子数, 的电子数为 56-2=54 , B 错误;
C .质子数为 35 、中子数为 45 的溴原子质量数为 35+45=80 : Br , C 正确;
D .中子数 = 质量数 - 质子数, Ti 的中子数是 48-22=26 , D 正确;
故选 B 。


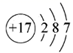 D
D