
根据相应信息回答有关问题。
I. 物质结构和规律推断
如图为周期表中短周期的一部分,已知 A 是地壳中含量最多的元素。
| | A | |
| B | C | D |
(1) 比较 A 、 C 的原子半径大小 _______( 用原子符号表示 ) 。
(2) 比较 C 、 D 的简单氢化物的稳定性 _______( 用化学式表示 ) 。
II. 实验操作和现象分析
(3) 配制 100ml0.1mol/L 的 NaOH 溶液时,若仰视定容,则所配溶液的物质的量浓度 _______( 填 “ 偏大 ” 、 “ 偏小 ” 或 “ 不变 ") 。
(4) 将适量 Ba(OH) 2 •8H 2 O 晶体与 NH 4 Cl 晶体放入烧杯中,用玻璃棒快速搅拌,试着拿起烧杯观察,晶体变成糊状,此外还可观察到 _______ 等现象。
III 物质性质和成分探究
(5) 将二氧化硫气体通入到品红溶液中,溶液褪色,体现了二氧化硫的 _______ 性。
(6) 在实验室,浓硝酸保存在棕色试剂瓶中,因浓硝酸见光或受热易分解,产生有刺激性气味的红棕色气体,该气体为 _______( 用化学式表示 ) 。
(1)O<S 或 S>O
(2)H 2 S<HCl 或 HCl>H 2 S
(3) 偏小
(4) 产生刺激性气味的气体,烧杯壁变冷
(5) 漂白
(6)NO 2
【解析】
【分析】
A 为地壳中含量最多的元素, A 为 O , C 为 S , B 为 P , D 为 Cl 。
( 1 ) O 与 S 为同主族元素,从上往下原子半径逐渐增大,故原子半径大小: O<S 或 S>O ;
( 2 )同周期从左往右非金属性增强,非金属性越强,简单气态氢化物越稳定,故 H 2 S<HCl 或 HCl>H 2 S ;
( 3 )若仰视容量瓶定容,加入水的体积偏大,配制溶液的浓度偏小;
( 4 )氯化铵与氢氧化钡反应生成氨气,且反应吸热,故产生刺激性气味的气体,烧杯壁变冷;
( 5 )二氧化硫使品红溶液褪色体现的是其漂白性;
( 6 )浓硝酸见光分解生成二氧化氮、氧气和水,红棕色气体为 NO 2 。

 2SO3
2SO3

二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:



SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表 ,如下数轴所示:
,如下数轴所示:
分析数轴可得:
(1) 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2) ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3) ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4) ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5) ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。



登录并加入会员可无限制查看知识点解析
下图中每个方框表示有关的一种反应物或生成物,方框中字母是物质代号,已知B、D、E、F、X均为单质,试填空。
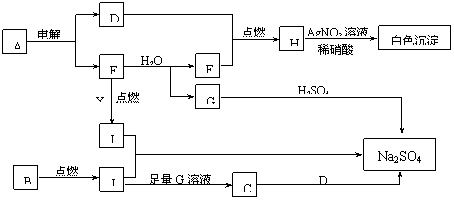 |
⑴写出A、B的化学:A___________,B____________。
⑵写出I和J反应的化学方程式__________________________________________。
写出E和水反应的离子方程式_________________________________________。
⑶写出C溶液和D反应的离子方程式_____________________________________。