亚硒酸钠 (Na 2 SeO 3 ) 为白色晶体,易溶于水,不溶于乙醇,有剧毒,可作为硒元素福补充药,在医学上可用于防治癌症、高血压、冠心病、心肌炎等疾病。
I. 工业上用烟气制酸的废料 ( 主要含 S 、 Se 、 Fe 2 O 3 、 CuO 、 ZnO 、 SiO 2 等 ) 为原料提取硒,流程如图:
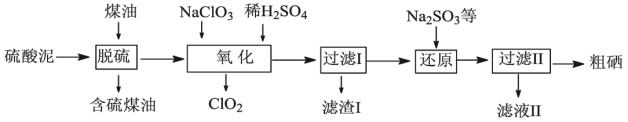
(1) 硒与硫是同主族的相邻元素,其在周期表中的位置是 _______ 。
(2)“ 脱硫 ” 过程中,温度控制在 95℃ ,原因是 _______ 。
(3)“ 氧化 ” 过程中, Se 转化成弱酸 H 2 SeO 3 ,该反应的离子方程式为 _______ 。
(4)“ 还原 ” 过程中,生成粗硒的离子方程式为 _______ 。
II. 粗硒经过下列流程可获得亚硒酸钠 (Na 2 SeO 3 ) 。
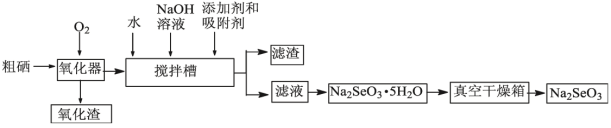
(5) 已知在氧化器中粗硒转化为 SeO 2 ,则搅拌槽中发生主要反应的离子方程式为 _______ 。
(6)Na 2 SeO 3 ·5H 2 O 脱水制取 Na 2 SeO 3 时,须在真空干燥箱中进行,原因是 _______ 。
(7) 在上述流程中粗硒在转化为 SeO 2 时损失 4% ,搅拌槽中 SeO 2 的利用率为 95% ,其他损耗忽略不计,则利用 1t 含硒 79% 的粗硒最终可生产 _______t 含亚硒酸钠 95% 的产品 ( 计算结果精确到 0.01t) 。
答案
(1) 第四周期第 ⅥA 族
(2) 温度低于 95℃ ,脱硫速率偏低(硫在煤油中的溶解度降低),温度高于 95℃ ,煤油挥发量加大
(3)Se+4 +4H + =H 2 SeO 3 +4ClO 2 ↑+H 2 O
(4)H 2 SeO 3 +2 =Se+2
+H 2 O
(5)SeO 2 +2OH - = +H 2 O
(6) 防止 Na 2 SeO 3 被空气中的氧气氧化
(7)1.66
【解析】
【分析】
I .向硫酸泥 ( 主要含 S 、 Se 、 Fe 2 O 3 、 CuO 、 ZnO 、 SiO 2 等 ) 中加入煤油,将硫溶解、除去; “ 氧化 ” 过程中,加入 NaClO 3 和 H 2 SO 4 , Se 转化为 H 2 SeO 3 , Fe 2 O 3 、 CuO 、 ZnO 转化为 Fe 3+ 、 Cu 2+ 、 Zn 2+ , “ 过滤 I” 除去 SiO 2 ;向滤液中加入 Na 2 SO 3 等, H 2 SeO 3 转化为 Se , Fe 3+ 转化为 Fe 2+ , “ 过滤 II” 获得粗硅;
II .粗硒在氧化器中被氧化为 SeO 2 ;在搅拌槽中, SeO 2 转化为 Na 2 SeO 3 ,过滤得到含 Na 2 SeO 3 的溶液,再结晶得到 Na 2 SeO 3 ∙5H 2 O ,并脱水得到 Na 2 SeO 3 。
( 1 )硒与硫是同主族的相邻元素,其在周期表中的位置是第四周期第 ⅥA 族;
( 2 ) “ 脱硫 ” 过程中,温度控制在 95℃ ,原因是温度低于 95℃ ,脱硫速率偏低(硫在煤油中的溶解度降低),温度高于 95℃ ,煤油挥发量加大;
( 3 ) “ 氧化 ” 过程中, Se 转化成弱酸 H 2 SeO 3 ,该反应的离子方程式为 Se+4 +4H + =H 2 SeO 3 +4ClO 2 ↑+H 2 O ;
( 4 ) “ 还原 ” 过程中, H 2 SeO 3 转化为 Se ,该反应的离子方程式为 H 2 SeO 3 +2 =Se+2
+H 2 O ;
( 5 )在搅拌槽中, SeO 2 转化为 Na 2 SeO 3 ,该反应的离子方程式为 SeO 2 +2OH - = +H 2 O ;
( 6 ) Na 2 SeO 3 具有还原性, Na 2 SeO 3 ·5H 2 O 脱水制取 Na 2 SeO 3 时,须在真空干燥箱中进行,是为了防止 Na 2 SeO 3 被空气中的氧气氧化;
( 7 )根据 Se 原子守恒,可知 Se~SeO 2 ~Na 2 SeO 3 , 1t 含硒 79% 的粗硒中, m (Se)=0.79t ,其转化为 Na 2 SeO 3 的质量 m (Na 2 SeO 3 )= =1.58t ,则利用 1t 含硒 79% 的粗硒最终可生产含亚硒酸钠 95% 的产品的质量为
=1.66t 。



