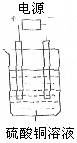
下列关于电解 CuCl 2 溶液 ( 如图所示 ) 的说法中,错误的是
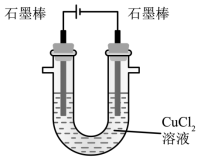
A .电解过程中, Cl — 向阳极移动
B .总反应为: CuCl 2 =Cu 2+ +2Cl —
C .阳极有黄绿色气体产生,并可用湿润的 KI 淀粉试纸检验
D .若将溶液换为硫酸铜溶液,则阴、阳两极得到单质的物质的量之比始终为 2∶1
答案
B
【解析】
【详解】
A .电解过程中,氯离子和氢氧根离子向阳极移动,故 A 正确;
B .氯化铜溶液电解生成铜和氯气,总反应方程式为 CuCl 2 Cu+ Cl 2 ↑ ,故 B 错误;
C .电解过程中,氯离子在阳极失去电子发生氧化反应生成黄绿色的氯气,氯气与碘化钾溶液反应生成的碘使淀粉溶液变蓝色,可用湿润的碘化钾淀粉试纸检验,故 C 正确;
D .若将溶液换为硫酸铜溶液,电解过程中,阴极析出的单质为铜、阳极析出的单质为氧气,硫酸铜溶液完全电解后继续电解,实质上是电解水,阴极析出的单质为氢气、阳极析出的单质为氧气,由得失电子数目守恒可知,铜和氧气的物质的量比与氢气和氧气的物质的量比相等,都是 2∶1 ,故 D 正确;
故选 B 。