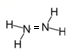
下列表示正确的是
A . 乙酸乙酯的实验式: C 2 H 4 O 2
B . 羰基的电子式: ![]()
C . 2— 甲基 —1 , 3— 丁二烯的分子式: C 5 H 10
D . 2 , 4 , 4— 三甲基己烷的键线式: ![]()
答案
D
【详解】
A .乙酸乙酯的实验式即最简式为: CH 2 O , A 错误;
B .羰基中 O 原子达到 8e 稳定结构, C 原子有 2 个孤电子, B 错误;
C . 2- 甲基 -1 , 3- 丁二烯,一共 5 个碳,二烯含有两个双键,不饱和度为 2 ,比饱和烃少 4 个 H ,所以分子式为: C 5 H 8 , C 错误;
D . ![]() 为烷烃的键线式,最长碳链含有 6 个 C 原子,主链为己烷,在 2 、 4 、 4 号碳原子各含有 1 个甲基,其名 2 , 4 , 4— 三甲基己烷, D 正确;
为烷烃的键线式,最长碳链含有 6 个 C 原子,主链为己烷,在 2 、 4 、 4 号碳原子各含有 1 个甲基,其名 2 , 4 , 4— 三甲基己烷, D 正确;
故选 D 。


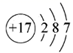 D
D