二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1) 二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的 _______
;若反应 ①为慢反应,下列示意图中能体现上述反应能量变化的是 _______ ( 填标号 ) ,判断的理由是 _______ 。
A. 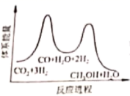 B.
B. 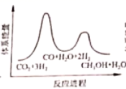 C.
C. 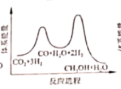 D.
D. 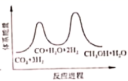
(2) 合成总反应在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
,在
℃ 下的
、在
下的
如图所示。
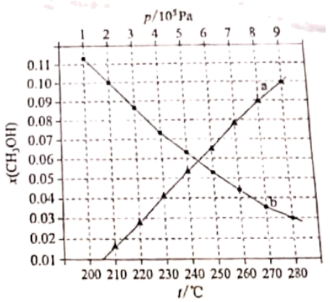
①用各物质的平衡分压表示总反应的平衡常数,表达式 _______ ;
②图中对应等压过程的曲线是 _______ ,判断的理由是 _______ ;
③当 时,
的平衡转化率
____ ,反应条件可能为 ___ 或 ___ 。
答案
-49 A Δ H 1 为正值, Δ H 2 为和 Δ H 为负值,反应 ①的活化能大于反应②的 b 总反应 Δ H <0 ,升高温度时平衡向逆反应方向移动,甲醇的物质的量分数变小 33.3% 5×10 5 Pa , 210℃ 9 × 10 5 Pa , 250 ℃
【详解】
(1) 二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现: ①
, ②
,根据盖斯定律可知, ① + ②可得二氧化碳加氢制甲醇的总反应为:
;该反应总反应为放热反应,因此生成物总能量低于反应物总能量,反应 ①为慢反应,因此反应①的活化能高于反应②,同时反应①的反应物总能量低于生成物总能量,反应②的反应物总能量高于生成物总能量,因此示意图中能体现反应能量变化的是 A 项,故答案为: -49 ; A ; Δ H 1 为正值, Δ H 2 为和 Δ H 为负值,反应 ①的活化能大于反应②的。
(2) ①二氧化碳加氢制甲醇的总反应为 ,因此利用各物质的平衡分压表示总反应的平衡常数,表达式 K p =
,故答案为:
。
②该反应正向为放热反应,升高温度时平衡逆向移动,体系中 将减小,因此图中对应等压过程的曲线是 b ,故答案为: b ;总反应 Δ H <0 ,升高温度时平衡向逆反应方向移动,甲醇的物质的量分数变小。
③设起始 n (CO 2 )=1mol , n (H 2 )=3mol ,则 ,当平衡时
时,
=0.1 ,解得 x=
mol ,平衡时 CO 2 的转化率 α=
=33.3% ;由图可知,满足平衡时
的条件有: 5×10 5 Pa , 210℃ 或 9×10 5 Pa , 250℃ ,故答案为: 33.3% ; 5×10 5 Pa , 210℃ ; 9×10 5 Pa , 250℃ 。