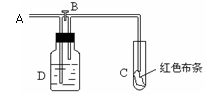
某学习小组通过下列装置探究 M n O 2 与 FeCl 3 ·6H 2 O 能否反应产生 Cl 2 。已知 FeCl 3 的升华温度为 315 ℃。

实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | i. 试管 A 中部分固体溶解,上方出现白雾 ii. 稍后,试管 A 中产生黄色气体,管壁附着黄色液滴 iii. 试管 B 中溶液变蓝 |
(1) 分析现象 ii ,该小组探究黄色气体的成分,实验如下:
a. 加热 FeCl 3 ·6H 2 O ,产生白雾和黄色气体。
b. 用 KSCN 溶液检验现象 ii 和实验 a 中的黄色气体,溶液均变红。
通过该实验说明现象 ii 中黄色气体含有 _______ ( 填化学式 ) 。
(2) 为进一步确认黄色气体是否含有 Cl 2 ,该小组提出以下方案,证实了 Cl 2 的存在:在 A 、 B 间增加盛有某种试剂的洗气瓶 C , B 中溶液变为蓝色。 C 中盛放的试剂是 _______ ( 填字母序号 ) 。
A.NaCl 饱和溶液 B.NaOH 溶液 C.NaHCO 3 饱和溶液
(3) 除了氯气可使 B 中溶液变蓝,可能的原因还有:在酸性条件下,装置中的空气使之变蓝。为探究 KI 浓度对该反应速率的影响,进行了如下实验,请完成下表的探究内容。
| 实验 | H 2 SO 4 溶液 | KI 溶液 | 淀粉溶液 | 蒸馏水 | ||
| 编号 | 浓度 /mol·L -1 | 体积 /mL | 浓度 /mol·L -1 | 体积 /mL | 体积 /mL | 体积 /mL |
| ① | 0.10 | ___ | 1.00 | 5.0 | 3.0 | 2.0 |
| ② | 0.10 | 2.0 | 1.00 | 3.0 | ___ | ___ |
| ③ | 0.10 | ___ | 1.00 | ___ | 3.0 | 6.0 |
混合上述试剂时,最后加入的试剂是 _______ 。
(4) 将试管 A 中的固体产物分离得到 Fe 2 O 3 固体和 MnCl 2 溶液。
①加热时 A 中产生 Cl 2 的化学方程式为: _______ ;
②把分离出的 MnCl 2 溶液配制成 100mL 溶液,从中取出 l0.00mL 溶液于锥形瓶中,加入几滴 K 2 CrO 4 溶液作指示剂,用 0.5000mol·L -1 的 AgNO 3 溶液滴定,至滴定终点时消耗 12.00mLAgNO 3 溶液。则混合 MnO 2 与 FeCl 3 ·6H 2 O 进行探究时,所需 MnO 2 的质量为 _______ g 。
答案
FeCl 3 A 2.0 3.0 4.0 2.0 1.0 稀硫酸 3MnO 2 + 4FeCl 3 ·6H 2 O Fe 2 O 3 + 3MnCl 2 + 3Cl 2 ↑ + 24H 2 O 2.610
【分析】
由题意可知,加热试管 A 中二氧化锰与六水氯化铁混合物时,二氧化锰与六水氯化铁反应生成氧化铁、氯化锰、氯气和水。
【详解】
(1) 铁离子遇硫氰化钾溶液,溶液会变为红色,用硫氰化钾溶液检验加热二氧化锰与六水氯化铁混合物和加热六水氯化铁中的黄色气体,溶液均变红说明黄色气体中含有氯化铁,故答案为: FeCl 3 ;
(2) 由题意可知,黄色气体中可能含有氯化氢、氯化铁和氯气,氯化铁能与碘化钾溶液发生氧化还原反应生成单质碘,会干扰氯气的检验,由于氯气能与氢氧化钠溶液和饱和碳酸氢钠溶液反应,则吸收黄色气体中氯化铁的试剂应选择饱和食盐水,故答案为: A ;
(3) 由变量唯一化的原则可知,探究碘化钾浓度对该反应速率的影响时,除碘化钾浓度发生改变外,稀硫酸溶液、淀粉溶液的浓度不能发生改变,则实验时稀硫酸溶液和淀粉溶液的体积必须相同,混合溶液的总体积要保持不变,实验 ①②③中稀硫酸溶液的体积都为 2.0mL 、淀粉溶液的体积都为 3.0mL ,混合溶液的总体积 12.0mL ,实验 ②中蒸馏水的体积为 12.0mL — 8.0mL=4.0mL ,实验 ③中碘化钾溶液的体积为 12.0mL — 11.0mL=1.0mL ;因在酸性条件下,装置中的空气使碘化钾溶液变蓝,为防止酸性条件下空气干扰实验,混合上述试剂时,应最后加入稀硫酸溶液,故答案为: 2.0 ; 3.0 ; 4.0 ; 2.0 ; 1.0 ;稀硫酸;
(4) ①由题给信息可知,试管 A 中发生的反应为二氧化锰与六水氯化铁反应生成氧化铁、氯化锰、氯气和水,反应的化学方程式为 3MnO 2 + 4FeCl 3 ·6H 2 O Fe 2 O 3 + 3MnCl 2 + 3Cl 2 ↑ + 24H 2 O ,故答案为: 3MnO 2 + 4FeCl 3 ·6H 2 O
Fe 2 O 3 + 3MnCl 2 + 3Cl 2 ↑ + 24H 2 O ;
②由题意可得二氧化锰和氯化银的关系为 MnO 2 — MnCl 2 — 2 AgNO 3 ,硝酸银的物质的量为 0.5000mol·L -1 × 0.01200L=6 × 10 — 3 mol ,则试管 A 中二氧化锰的质量为 6 × 10 — 3 mol × × 10 × 87g/mol=2.610g ,故答案为: 2.610 。




 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。  2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。  HCl+HClO
HCl+HClO