我国科研人员提出了由 CO 2 和 CH 4 转化为高附加值产品 CH 3 COOH 的催化反应历程,该历程示意图如下所示。
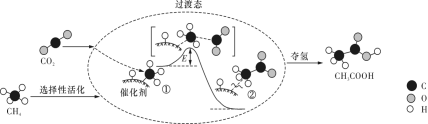
下列说法不正确的是
A . 生成 CH 3 COOH 总反应的原子利用率为 100%
B . CH 4 →CH 3 COOH 过程中,有 C—H 键发生断裂
C . ① → ②放出能量并形成了 C—C 键
D . 该催化剂可有效提高反应物的平衡转化率
答案
D
【解析】
分析 : A 项,生成 CH 3 COOH 的总反应为 CH 4 +CO 2 ![]() CH 3 COOH ,原子利用率为 100%;B 项, CH 4 选择性活化变为 ① 过程中,有 1 个 C-H 键发生断裂; C 项,根据图示, ① 的总能量高于 ② 的总能量, ①→② 放出能量并形成 C-C 键 ; D 项,催化剂只影响化学反应速率,不影响化学平衡,不能提高平衡转化率 。
CH 3 COOH ,原子利用率为 100%;B 项, CH 4 选择性活化变为 ① 过程中,有 1 个 C-H 键发生断裂; C 项,根据图示, ① 的总能量高于 ② 的总能量, ①→② 放出能量并形成 C-C 键 ; D 项,催化剂只影响化学反应速率,不影响化学平衡,不能提高平衡转化率 。
详解 : A 项,根据图示 CH 4 与 CO 2 在催化剂存在时生成 CH 3 COOH ,总反应为 CH 4 +CO 2 ![]() CH 3 COOH, 只有 CH 3 COOH 一种生成物,原子利用率为 100%,A 项正确; B 项, CH 4 选择性活化变为 ① 过程中,有 1 个 C-H 键发生断裂 , B 项正确; C 项,根据图示, ① 的总能量高于 ② 的总能量, ①→② 放出能量 , 对比 ① 和 ②,①→② 形成 C-C 键 , C 项正确 ; D 项,催化剂只影响化学反应速率,不影响化学平衡 , 不能提高反应物的平衡转化率, D 项错误;答案选 D。
CH 3 COOH, 只有 CH 3 COOH 一种生成物,原子利用率为 100%,A 项正确; B 项, CH 4 选择性活化变为 ① 过程中,有 1 个 C-H 键发生断裂 , B 项正确; C 项,根据图示, ① 的总能量高于 ② 的总能量, ①→② 放出能量 , 对比 ① 和 ②,①→② 形成 C-C 键 , C 项正确 ; D 项,催化剂只影响化学反应速率,不影响化学平衡 , 不能提高反应物的平衡转化率, D 项错误;答案选 D。
点睛:本题考查原子利用率、化学反应的实质、化学反应中的能量变化、催化剂对化学反应的影响,解题的关键是准确分析示意图中的信息。注意催化剂能降低反应的活化能,加快反应速率,催化剂不能改变 ΔH、 不能使化学平衡发生移动。
