为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
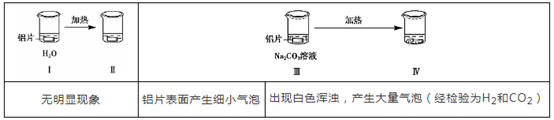
下列说法不正确的是( )
A.Na2CO3溶液中存在水解平衡:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
B.对比Ⅰ、Ⅲ,推测Na2CO3溶液能破坏铝表面的氧化膜
C.Ⅳ溶液中可能存在大量Al3+
D.推测出现白色浑浊的可能原因:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
答案
C
【解析】
A. 溶液中碳酸根会水解,结合水电出来的氢离子,生成碳酸氢根,选项A正确;
B.实验Ⅰ和Ⅱ没有气泡,根据所学Al可以和热水反应,但是此实验中没有气泡,说明有氧化膜的保护,实验Ⅲ中却有气泡,说明氧化膜被破坏,选项B正确;
C.Ⅳ溶液中出现白色沉淀,白色沉淀应该为氢氧化铝,则不可能存在大量Al3+,选项C不正确;
D.Na2CO3溶液呈碱性,铝片在碱性溶液中与OH-反应,生成偏铝酸根,2Al+2OH-+2H2O=2AlO2-+3H2↑,AlO2-和HCO3-反应生成氢氧化铝沉淀,选项D正确;
答案选C。

 ” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。 

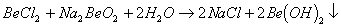 能完全进行,则下列推断中,正确的是
能完全进行,则下列推断中,正确的是 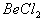 溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO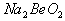 溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO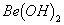 既能溶于盐酸又能溶于烧碱溶液
既能溶于盐酸又能溶于烧碱溶液