下列装置能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 |
|
|
|
|
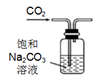
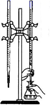
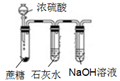
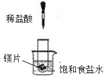
| 实验目的 | 探究Na2CO3和NaHCO3溶解度的相对大小 | 用已知浓度的NaOH溶液滴定未知浓度的稀硫酸 | 检验蔗糖与浓硫酸反应产生的CO2 | 验证镁和稀盐酸的反应的热效应 |
A.A B.B C.C D.D
答案
A
【分析】
A.向饱和碳酸钠溶液中通入二氧化碳,可析出碳酸氢钠;
B.NaOH会与酸式滴定管中的SiO2反应;
C.CO2、SO2都能使澄清石灰水变浑浊;
D.检验Mg与盐酸反应放出热量的现象不明显。
【详解】
A.向饱和碳酸钠溶液中通入二氧化碳,可析出碳酸氢钠,可探究Na2CO3和NaHCO3溶解度相对大小,A.正确;
B.用已知浓度的NaOH溶液滴定未知浓度的稀硫酸NaOH,NaOH 溶液应该使用碱式滴定管,若使用酸式滴定管,会与玻璃中SiO2反应产生Na2SiO3,将滴定管与旋塞黏在一起,使滴定管报废,B错误;
C.浓硫酸具有脱水性,能够使蔗糖脱水碳化,浓硫酸还具有强的氧化性,将反应产生的C单质氧化产生CO2,浓硫酸被还原产生SO2,CO2、SO2都能与Ca(OH)2反应产生白色难溶性的物质,因此都可以使澄清石灰水变浑浊,故不能检验CO2气体,C错误;
D.Mg与盐酸产生氯化镁和氢气,反应放出热量,但由于氯化钠的溶解度随温度升高而稍有增大,且没有使用温度计,所以饱和食盐水中无明显现象,无法证明反应放热,D错误;
故合理选项是A。
【点睛】
本题考查化学实验方案的评价的知识。注意滴定管使用时,碱式滴定管盛装碱性溶液,酸式滴定管盛装酸性和氧化性的物质,对于D选项,可以将饱和食盐水改为饱和的澄清石灰水,利用Ca(OH)2的溶解度随温度的升高而降低的性质,若看到石灰水变浑浊,就可以证明镁和稀盐酸的反应是放热反应,易错点是选项C,只清楚可以用澄清石灰水检验CO2,忽视了SO2与Ca(OH)2反应产生的CaSO3也是白色难溶性的物质的性质。可见掌握常见的物质的物理性质也是物质鉴别中不容忽视的知识点。