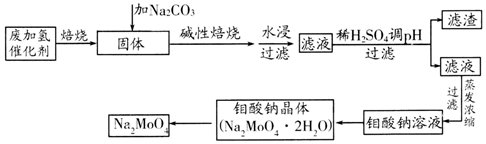
钼酸钠(Na2MoO4)是一种重要的化工原料。用废加氢催化剂(含有MoS2和Al2O3、Fe2O3、SiO2等)为原料制取钼酸钠,工艺流程如图所示:
已知:MoO3、A12O3在高温下能跟Na2CO3发生反应。
回答下列问题:
(1)Na2MoO4中Mo元素的化合价______。
(2)废加氢催化剂焙烧目的是脱除表面油脂、硫等。请根据表中实验数据分析,废加氢催化剂预处理温度应选择______℃。
废催化剂在不同温度下的烧残(时间:2h)
| 温度 /℃ | 300 | 350 | 400 | 500 | 600 |
| 烧前 /g | 50.00 | 50.00 | 50.00 | 50.00 | 50.00 |
| 烧后 /g | 48.09 | 47.48 | 47.19 | 46.55 | 46.52 |
| 烧残, % | 96.2 | 95.0 | 94.4 | 93.1 | 93.0 |
(3)焙烧时生成MoO3的化学方程式为______,当生成1mol MoO3转移电子数为______NA。
(4)加碳酸钠碱性焙烧时主要反应的化学方程式为______。
(5)用50t含MoS2为80%的废加氢催化剂,经过制取、分离、提纯,得到30.9t Na2MoO4,则Na2MoO4的产率为______。
答案
+6 500 2MoS2+7O2![]() 2MoO3+4SO2 14 MoO3+Na2CO3
2MoO3+4SO2 14 MoO3+Na2CO3![]() Na2MoO4+CO2↑ 60%
Na2MoO4+CO2↑ 60%
【分析】
根据流程:空气中焙烧废加氢催化剂,MoS2燃烧反应方程式为2MoS2+7O2![]() 2MoO3+4SO2,加Na2CO3碱性焙烧,再加水溶解过滤所得滤液,然后向滤液中加入稀硫酸调节pH值,过滤,溶液中的溶质为Na2MoO4,所以加碳酸钠碱性焙烧时主要是将MoO3转化为易溶于水的Na2MoO4,反应的化学方程式为MoO3+Na2CO3
2MoO3+4SO2,加Na2CO3碱性焙烧,再加水溶解过滤所得滤液,然后向滤液中加入稀硫酸调节pH值,过滤,溶液中的溶质为Na2MoO4,所以加碳酸钠碱性焙烧时主要是将MoO3转化为易溶于水的Na2MoO4,反应的化学方程式为MoO3+Na2CO3![]() Na2MoO4+CO2↑,将溶液蒸发浓缩、冷却结晶,得到Na2MoO4•2H2O晶体,再分解得到Na2MoO4,据此分析作答。
Na2MoO4+CO2↑,将溶液蒸发浓缩、冷却结晶,得到Na2MoO4•2H2O晶体,再分解得到Na2MoO4,据此分析作答。
【详解】
(1)根据Na2MoO4中化合价代数和为0,Mo元素的化合价为+(2×4-1×2)=+6价;
故答案为:+6;
(2)由废加氢催化剂焙烧目的是脱除表面油脂、硫等,结合表中实验数据可知,500℃后烧残的百分含量几乎不变,所以废加氢催化剂预处理温度应选择500℃,故答案为:500;
(3)空气中焙烧废加氢催化剂,MoS2燃烧反应生成MoO3的化学方程式为2MoS2+7O2![]() 2MoO3+4SO2,反应中Mo元素化合价由+4价升高到+6,S元素化合价由-2升高到+4,则由方程式可知转移电子数为2×(6-4+2×6)=28e-,所以当生成1mol MoO3转移电子数为14NA;
2MoO3+4SO2,反应中Mo元素化合价由+4价升高到+6,S元素化合价由-2升高到+4,则由方程式可知转移电子数为2×(6-4+2×6)=28e-,所以当生成1mol MoO3转移电子数为14NA;
故答案为:2MoS2+7O2![]() 2MoO3+4SO2;14;
2MoO3+4SO2;14;
(4)加碳酸钠碱性焙烧时主要是将MoO3转化为易溶于水的Na2MoO4,反应的化学方程式为MoO3+Na2CO3![]() Na2MoO4+CO2↑;
Na2MoO4+CO2↑;
故答案为:MoO3+Na2CO![]() Na2MoO4+CO2↑;
Na2MoO4+CO2↑;
(5)用50t含MoS2为80%的废加氢催化剂,则含MoS2的物质的量为![]() =2.5×105mol,根据Mo原子守恒n(Mo)=n(MoS2)=n(Na2MoO4),所以Na2MoO4的产率=
=2.5×105mol,根据Mo原子守恒n(Mo)=n(MoS2)=n(Na2MoO4),所以Na2MoO4的产率=![]() ×100%=60%,故答案为:60%。
×100%=60%,故答案为:60%。
【点睛】
本题考查了物质制备流程和方案的分析判断,物质性质的应用,题干信息的分析理解,结合题目信息对流程的分析是本题的解题关键,需要学生有扎实的基础知识的同时,还要有处理信息应用的能力,注意对化学平衡常数的灵活运用,综合性强。


