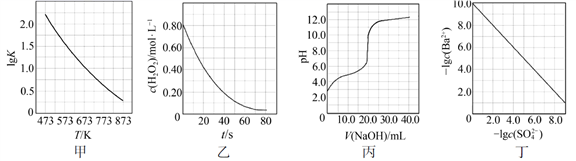
下列图示与对应的叙述相符的是

A.图1表示1 LpH=2的CH3COOH溶液加水稀释至V L,pH随lgV的变化
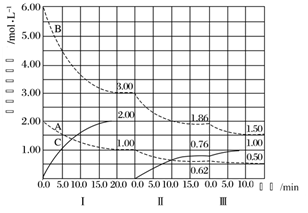
B.图2表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度T2>T1
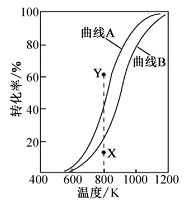
C.图3表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率小于b点
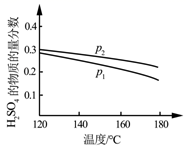
D.图4表示同一温度下,在不同容积的容器中进行反应2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
答案
C
【详解】
A、CH3COOH是弱酸,溶液中存在电离平衡,所以加水稀释时电离程度增大,但离子浓度是减小的,若溶液体积增大10倍,c(H+)大于原来的1/10,所以pH的变化量小于1,故A错误;
B、水的电离是吸热的,所以升高温度,电离出的H+和OH-浓度增大,所以图象中的温度为T1>T2,所以B错误;
C、由图象可知在N2的起始量恒定时,随H2量的增加,N2的转化率增大,所以a点N2的转化率小于b点,故C正确;
D、容器体积的增大,即减小压强,平衡向气体体积增大的方向移动,即该平衡正向移动,温度不变时平衡常数不变,故O2的平衡浓度是不变,所以D错误。
本题正确答案为C。

 pC(g)+qD(g)
pC(g)+qD(g)  。
。 时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。
时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。 指的是同一物质的正反应速率与逆反应速率相等。
指的是同一物质的正反应速率与逆反应速率相等。  qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。
qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。