许多含氮物质会造成环境污染,硝酸工业的尾气(含NO、NO2)会造成大气污染,通常用选择性非催化还原法或碱液吸收法[石灰乳吸收,既能净化尾气,又能获得应用广泛的Ca(NO2)2]。而废水中过量的氨氮(NH3和NH4+)会导致水体富营养化,则通常用强氧化剂来吸收。
(1)废气中氮氧化物的吸收。
①选择性非催化还原法。发生的主要反应有:
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1
4N2(g)+6H2O(g) ΔH=-1646 kJ·mol-1
2NO(g)+(NH2)2CO(s)+![]() O2(g)
O2(g)![]() 2N2(g)+2H2O(g)+CO2(g) ΔH=-780.02 kJ·mol-1
2N2(g)+2H2O(g)+CO2(g) ΔH=-780.02 kJ·mol-1
则2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的ΔH=__________。
CO(NH2)2(s)+H2O(g)的ΔH=__________。
②碱液吸收法。该工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),得到的滤渣可循环使用,该滤渣的主要成分是________(填化学式)。 工艺需控制NO和NO2物质的量之比接近__________,若小于这个比值,则会导致_______________。
(2)废水中过量的氨氮(NH3和NH4+)处理。某科研小组用NaClO氧化法处理氨氮废水。
已知:A.HClO的氧化性比NaClO强;
B.NH3比NH4+更易被氧化;
C.国家标准要求经处理过的氨氮废水pH要控制在6~9。
进水pH对氨氮去除率的影响如下图所示。
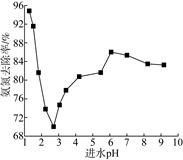
①进水pH为2.75~6.00范围内,氨氮去除率随pH升高而上升的原因是___________。
②写出酸性条件下ClO-氧化NH4+的离子方程式____________________。
③已知a.O2的氧化性比NaClO弱; b.O2氧化氨氮速率比NaClO慢。
在其他条件不变时,仅增加单位时间内通入空气的量,氨氮去除率_______________(填“显著变大”“显著变小”或“几乎不变”)。
答案
-42.98 kJ/mol Ca(OH)2 1∶1 Ca(NO2)2中杂质Ca(NO3)2的含量偏高 随着pH升高,氨氮废水中NH3含量增大,氨氮更易被氧化 3ClO-+2NH4+=N2↑+3Cl-+3H2O+2H+(或写为3HClO+2NH4+=N2↑+3Cl-+3H2O+5H+) 几乎不变
【分析】
(1)①根据盖斯定律,将已知热化学方程式叠加,可得2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的反应热;
CO(NH2)2(s)+H2O(g)的反应热;
②根据硝酸工业的尾气(含NO、NO2)与Ca(OH)2反应产生Ca(NO2)2,石灰乳中含大量Ca(OH)2,过量的Ca(OH)2会导致物质不纯,结合NO2与Ca(OH)2反应产生的物质成分分析工艺需控制NO和NO2物质的量之比及作用;
(2)①根据废水中溶液pH大小与其中含有的NH3、NH4+的多少及NH3比NH4+更易被氧化分析;
②酸性条件下ClO-氧化NH4+为N2,ClO-被还原产生Cl-;
③根据已知条件a. O2的氧化性比NaClO弱;
b. O2氧化氨氮速率比NaClO慢进行分析判断。
【详解】
(1)①已知反应:(i)4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) ΔH=-1646 kJ/mol;
4N2(g)+6H2O(g) ΔH=-1646 kJ/mol;
(ii)2NO(g)+(NH2)2CO(s)+![]() O2(g)
O2(g)![]() 2N2(g)+2H2O(g)+CO2(g) ΔH=-780.02 kJ/mol,
2N2(g)+2H2O(g)+CO2(g) ΔH=-780.02 kJ/mol,
由于反应过程中的能量变化只与物质的始态和终态有关,与反应过程无关,根据盖斯定律,将(i)×![]() -(ii),整理可得2NH3(g)+CO2(g)
-(ii),整理可得2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的反应热ΔH= -42.98 kJ/mol;
CO(NH2)2(s)+H2O(g)的反应热ΔH= -42.98 kJ/mol;
②NO、NO2与Ca(OH)2会发生归中反应:NO+NO2+Ca(OH)2=Ca(NO2)2+H2O,由于Ca(NO2)2易溶于水,Ca(OH)2微溶于水,且石灰乳中Ca(OH)2主要以固体形式存在,导致不能与气体充分接触,使最后得到的滤渣中含有Ca(OH)2;根据方程式NO+NO2+Ca(OH)2=Ca(NO2)2+H2O可知:要制取Ca(NO2)2,应该控制NO、NO2的物质的量的比是1:1,若小于这个比值,则NO2气体过量,会发生反应:4NO2+2Ca(OH)2=Ca(NO3)2+Ca(NO2)2+2H2O,使Ca(NO2)2中杂质Ca(NO3)2的含量偏高;若大于这个比值,NO不能完全被吸收,仍然会导致大气污染;
(2)①废水中溶液pH越大,其中含有的NH3含量就越高,由于NH3比NH4+更易被氧化,因此氨氮更易被氧化;
②在酸性条件下ClO-、NH4+发生氧化还原反应产生N2、Cl-,根据电子守恒、电荷守恒、原子守恒,可得该反应的离子方程式为:3ClO-+2NH4+=N2↑+3Cl-+3H2O+2H+(或写为3HClO+2NH4+=N2↑+3Cl-+3H2O+5H+);
③由于a.O2的氧化性比NaClO弱;b.O2氧化氨氮速率比NaClO慢,因此在其他条件不变时,仅增加单位时间内通入空气的量,氨氮去除率几乎不变。
【点睛】
本题考查了反应热的计算及含氮物质造成环境污染的处理方法,掌握盖斯定律的含义及物质的性质,充分利用题干信息分析解答。大气中氮氧化合物会造成酸雨、光化学烟雾,污水中氮化合物增多,会使污水富营养化,而产生赤潮、水华现象,治理措施要结合氮的存在形式采用不同措施。若是氮氧化合物,一般采用碱液吸收方法,通常使用价廉、易得的石灰乳;废水中过量的氨氮一般采用氧化剂氧化方法处理,要尽量使物质变化的过程中能量得以充分利用,使废物资源化,做到物尽其用。



