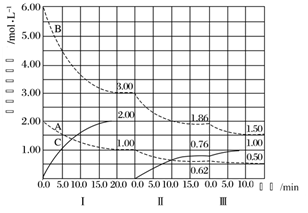
反应aA(g)+bB(g)![]() cC(g)ΔH<0在体积一定容器中进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)ΔH<0在体积一定容器中进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
(1)上述化学方程式中化学计量数b为___。
(2)用A的浓度变化表示三个阶段的平均反应速率,则vⅠ(A)、vⅡ(A)、vⅢ(A)中最小的是___。
(3)三个阶段的转化率依次αⅠ(B)、αⅡ(B)、αⅢ(B),它们由大到小的顺序为___。
(4)由第一次平衡到第二次平衡,采取的措施是___。
(5)比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低并说明理由:___。
答案
3 vⅢ(A) αⅠ(B)>αⅡ(B)>αⅢ(B) 从平衡混合物中分离出了C >,Ⅱ→Ⅲ平衡正向移动,该反应为放热反应,降温才能达到此目的
【分析】
第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动;第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低,以此解答。
【详解】
(1)由图可知第Ⅰ阶段,平衡时△c(A)=2mol/L-1mol/L=1mol/L,△c(B)=6mol/L-3mol/L=3mol/L,△c(C)=2mol/L,浓度变化量之比等于化学计量数之比,故a:b:c=1mol/L:3mol/L:2mol/L=1:3:2,化学计量数b为:3;
(2)vⅠ(A)=![]() =0.05mol/(L•min),vⅡ(A)=
=0.05mol/(L•min),vⅡ(A)=![]() =0.0253mol/(L•min),
=0.0253mol/(L•min),
vⅢ(A)=![]() =0.012mol/(L•min),故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A),则vⅠ(A)、vⅡ(A)、vⅢ(A)中最小的是:vⅢ(A);
=0.012mol/(L•min),故A的平均反应速率vⅠ(A)>vⅡ(A)>vⅢ(A),则vⅠ(A)、vⅡ(A)、vⅢ(A)中最小的是:vⅢ(A);
(3)B的平衡转化率αⅠ(B)=![]() ×100%=50%,αⅡ(B)=
×100%=50%,αⅡ(B)=![]() ×100%=38%,αⅢ(B)=
×100%=38%,αⅢ(B)=![]() ×100%=19.4%,由大到小的顺序为:αⅠ(B)>αⅡ(B)>αⅢ(B);
×100%=19.4%,由大到小的顺序为:αⅠ(B)>αⅡ(B)>αⅢ(B);
(4)第Ⅱ阶段C是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动,故答案为:从平衡混合物中移出产物C;
(5)第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据平衡开始时浓度确定此平衡移动不可能是由浓度的变化引起的,另外题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,另外结合A的速率在三个阶段的情况,确定改变的条件一定为降低温度,根据勒夏特列原理,平衡的移动只能减弱改变,不能抵消改变,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低,故答案为:>,Ⅱ→Ⅲ平衡正向移动,该反应为放热反应,降温才能达到此目的。

 pC(g)+qD(g)
pC(g)+qD(g)  。
。 时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。
时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。 指的是同一物质的正反应速率与逆反应速率相等。
指的是同一物质的正反应速率与逆反应速率相等。  qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。
qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。