(1)3.01×1023个OH-的物质的量为________mol,含有电子的物质的量为_______mol,这些OH-所含的电子数和_________g Na+含有的电子数相同。
(2)18.4g氮的氧化物N2Ox中含氮原子0.4mol,则N2Ox的摩尔质量为________;x=______。
答案
0.5 5 11.5 92g/mol 4
【分析】
利用n=![]() =
=![]() 进行计算。
进行计算。
【详解】
(1)根据n=![]() 可知,3.01×1023个OH-的物质的量为0.5mol;l个OH-含有10个电子,所以0.5molOH-含有电子的物质的量为5mol;l个Na+含有10个电子,则10×
可知,3.01×1023个OH-的物质的量为0.5mol;l个OH-含有10个电子,所以0.5molOH-含有电子的物质的量为5mol;l个Na+含有10个电子,则10×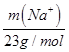 =5mol,m(Na+)=11.5g。
=5mol,m(Na+)=11.5g。
(2)18.4g氮的氧化物N2Ox中含氮原子0.4mol,一个分子中含有2个氮原子,则N2Ox的物质的量是0.2mol,所以其摩尔质量为M=![]() =
=![]() =92g/mol,因此x=
=92g/mol,因此x=![]() =4。
=4。
