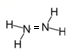
下列物质的电子式书写正确的是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
答案
D
【解析】
A.氨气为共价化合物,每个氢原子与氮原子形成一个共用电子对,氮原子最外层达到8电子稳定结构,电子式为![]() ,故A错误;
,故A错误;
B.氯气中氯原子之间形成一个共用电子对,每个氯原子最外层达到8电子稳定结构,Cl2的电子式![]() ,故B错误;
,故B错误;
C.二氧化碳中,每个氧原子与碳原子形成2个共用电子对,每个原子最外层都达到8电子稳定结构,则电子式为![]() ,故C错误;
,故C错误;
D.氯化钠是离子化合物,由钠原子失去电子变为钠离子,氯原子得到电子变为氯离子,电子式为![]() ,故D正确;
,故D正确;
答案选D。


 D
D