某同学对教材中铜与浓硫酸的实验作出如下改进。实验装置如图所示(加热和夹持装置已略去)。
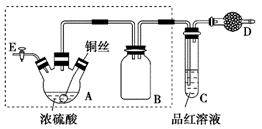
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是____________________________。
(2)装置A的名称是________,装置B的作用是_________,装置D中所盛药品是__________。
(3)装置A中发生反应的化学方程式为____________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是__________。
(5)实验后装置A中有白色固体产生,将装置A中固液混合物缓慢转移至盛有少量水的烧杯中,可观察到的现象是______________;不可直接向装置A中加水的原因是__________。
答案
(1). 关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变 (2). 三颈烧瓶; (3). 防倒吸 (4). 碱石灰 (5). Cu+2H2SO4═CuSO4+SO2↑+2H2O (6). 打开旋塞E,从E管口向A中鼓入大量空气 (7). 混合时放热,白色固体溶解,溶液变蓝色 (8). 水加入浓硫酸中,放出大量热使液体飞溅
【解析】
(1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;
(2)仪器A的名称是三颈烧瓶,仪器B的作用是防止二氧化硫倒吸,仪器D是处理尾气,而二氧化硫是酸性气体,所以D中所盛药品是碱石灰或NaOH固体;
(3)铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫和水;
(4)从E处鼓入空气或氮气,使体系中的二氧化硫完全除净;
(5)硫酸铜晶体溶于水溶液变蓝色;铜元素的焰色反应呈黄绿色,水加入浓硫酸中,放出大量热使液体飞溅.
【详解】(1)对于简易装置的气密性检查时,一般对瓶内气体加热,然后看有无气泡冒出或冷却后看导管口是否形成一段水柱,所以要关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变;
故答案为关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变;
(2)仪器A的名称是三颈烧瓶,仪器B的作用是防止二氧化硫倒吸,仪器D是尾气处理,而二氧化硫是酸性气体,所以D中所盛药品是碱石灰或NaOH固体;
故答案为三颈烧瓶;防倒吸;碱石灰;
(3)铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4═CuSO4+SO2↑+2H2O;
故答案为Cu+2H2SO4═CuSO4+SO2↑+2H2O;
(4)从E处鼓入空气或氮气,使体系中的二氧化硫完全除净,所以操作为:打开旋塞E,从E管口向A中鼓入大量空气,故答案为打开旋塞E,从E管口向A中鼓入大量空气;
(5)硫酸铜晶体溶于水溶液变蓝色;水加入浓硫酸中,放出大量热使液体飞溅;
故答案为混合时放热,白色固体溶解,溶液变蓝色;水加入浓硫酸中,放出大量热使液体飞溅。