氨是重要的基础化工原料,可以制备尿素[CO(NH2)2]、N2H4等多种含氮的化工产品。
(1)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:![]()
反应Ⅱ:![]()
反应Ⅲ:H2O(1)=H2O(g) △H3=+44.0 kJ·mol-1
则反应:![]() __________kJ/mol
__________kJ/mol
(2)将氨气与二氧化碳在有催化剂的反应器中反应![]() ,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
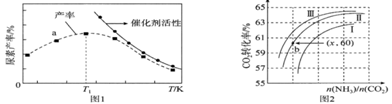
①a点________(填是或不是)处于平衡状态,T1之后尿素产率下降的原因是___________________________。
②实际生产中,原料气带有水蒸气,图2表示CO2![]() 转化率与氨碳比
转化率与氨碳比![]() 、水碳比
、水碳比![]() 的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是___________,测得b点氨的转化率为30%,则x=___________________。
的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是___________,测得b点氨的转化率为30%,则x=___________________。
③已知该反应的![]() ,
,![]() ,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是____________________________________。
,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是____________________________________。
(3)N2H4可作火箭推进剂。已知25℃时N2H4水溶液呈弱碱性:
![]() ;
;
![]()
①25℃时,向N2H4水溶液中加入H2SO4,欲使![]() ,同时
,同时![]() ,应控制溶液pH范围_____________(用含a、b式子表示)。
,应控制溶液pH范围_____________(用含a、b式子表示)。
②水合肼(N2H4·H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为_______________。
答案
(1). -87.0 (2). 不是 (3). 升高温度反应逆向移动;催化剂活性降低 (4). Ⅰ (5). 4 (6). ![]() (7). 14-b<pH<14-a (8). N2H6(HSO4)2
(7). 14-b<pH<14-a (8). N2H6(HSO4)2
【解析】(1)已知:
反应I:![]()
反应Ⅱ:![]()
反应Ⅲ:H2O(1)=H2O(g) △H3=+440 kJ·mol-1
NH3与CO2合成尿素同时生成液态水的化学方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(l),根据盖斯定律I+II-III得2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(l),则△H=-159.5kJ•mol-1+(+116.5kJ•mol-1)-(+44.0kJ•mol-1)=-87.0 kJ•mol-1;
(2)①产率最高之前,未达到平衡状态,反应为放热反应,达到平衡之后,升高温度,平衡逆向移动,产率下降,且催化剂活性降低;
②氨碳比相同时曲线Ⅲ二氧化碳的转化率大,所以曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是为Ⅰ;由题意可知:
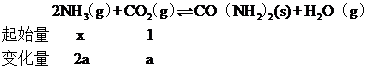
即![]() ,
,![]() =0.6,则x=4;
=0.6,则x=4;
③当V正=V逆时反应达到平衡,即![]() ,此时平衡常数K=
,此时平衡常数K=![]() =
=![]() ;
;
(3)①N2H4+H2O⇌N2H5++OH- K1=1×10-a;N2H5++H2O⇌N2H62++OH- K2=1×10-b,可知K1= 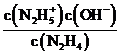 =1×10-a,K2=
=1×10-a,K2= 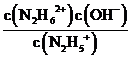 =1×10-b,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),则1×10-b<c(OH-)<1×10-a,即应控制溶液pH范围为14-b<pH<14-a;
=1×10-b,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),则1×10-b<c(OH-)<1×10-a,即应控制溶液pH范围为14-b<pH<14-a;
②既然水合肼的性质类似一水合氨,在水中应该能电离产生N2H62+和OH-,因此它的硫酸酸式盐的化学式为(N2H6)(HSO4)2。
【点睛】通常应用盖斯定律进行简单计算的基本方法是参照新的热化学方程式(目标热化学方程式),结合原热化学方程式(一般2~3个)进行合理“变形”,如热化学方程式颠倒、乘除以某一个数,然后将它们相加、减,得到目标热化学方程式,求出目标热化学方程式的ΔH与原热化学方程式之间ΔH的换算关系。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L