研究![]() 氧化
氧化![]() 制
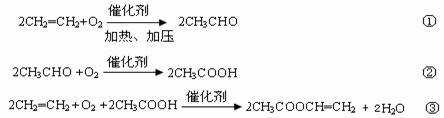
制![]() 对资源综合利用有重要意义。相关的主要化学反应有:
对资源综合利用有重要意义。相关的主要化学反应有:
Ⅰ ![]()
![]()
Ⅱ ![]()
![]()
Ⅲ ![]()
![]()
Ⅳ ![]()
![]()
已知:![]() 时,相关物质的相对能量(如图1)。
时,相关物质的相对能量(如图1)。

可根据相关物质的相对能量计算反应或变化的![]() (
(![]() 随温度变化可忽略)。例如:
随温度变化可忽略)。例如: ![]()
![]() 。
。
请回答:
(1)①根据相关物质的相对能量计算![]() _____
_____![]() 。
。
②下列描述正确的是_____
A 升高温度反应Ⅰ的平衡常数增大
B 加压有利于反应Ⅰ、Ⅱ的平衡正向移动
C 反应Ⅲ有助于乙烷脱氢,有利于乙烯生成
D 恒温恒压下通水蒸气,反应Ⅳ的平衡逆向移动
③有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:![]()
![]()
![]() ,且第二步速率较慢(反应活化能为
,且第二步速率较慢(反应活化能为![]() )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量-反应过程图”,起点从![]() 的能量
的能量![]() ,开始(如图2)_____
,开始(如图2)_____
。
(2)①![]() 和
和![]() 按物质的量1:1投料,在
按物质的量1:1投料,在![]() 和保持总压恒定的条件下,研究催化剂X对“
和保持总压恒定的条件下,研究催化剂X对“![]() 氧化
氧化![]() 制
制![]() ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:
| 催化剂 | 转化率 | 转化率 | 产率 |
| 催化剂X | 19.0 | 37.6 | 3.3 |
结合具体反应分析,在催化剂X作用下,![]() 氧化
氧化![]() 的主要产物是______,判断依据是_______。
的主要产物是______,判断依据是_______。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高![]() 的选择性(生成
的选择性(生成![]() 的物质的量与消耗
的物质的量与消耗![]() 的物质的量之比)。在
的物质的量之比)。在![]() ,乙烷平衡转化率为
,乙烷平衡转化率为![]() ,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到
,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到![]() 。结合具体反应说明乙烷转化率增大的原因是_____。
。结合具体反应说明乙烷转化率增大的原因是_____。
答案
(1). 430 (2). AD (3). 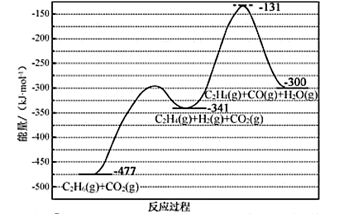 (4).
(4). ![]() (5).
(5). ![]() 的产率低,说明催化剂X有利于提高反应Ⅲ速率 (6). 选择性膜吸附
的产率低,说明催化剂X有利于提高反应Ⅲ速率 (6). 选择性膜吸附![]() ,促进反应Ⅱ平衡正向移动
,促进反应Ⅱ平衡正向移动
【解析】
【分析】
根据题中信息用相对能量求反应热;根据平衡移动原理分析温度、压强和反应物的浓度对化学平衡的影响,并作出相关的判断;根据相关物质的相对能量和活化能算出中间产物、过渡态和最终产物的相对能量,找到画图的关键数据;催化剂的选择性表现在对不同反应的选择性不同;选择性膜是通过吸附目标产品而提高目标产物的选择性的,与催化剂的选择性有所区别。
【详解】(1)①由图1的数据可知,C2H6(g)、CO2(g)、CO(g)、H2(g)的相对能量分别为-84kJ∙mol-1、-393 kJ∙mol-1、-110 kJ∙mol-1、0 kJ∙mol-1。由题中信息可知,∆H=生成物的相对能量-反应物的相对能量,因此,C2H6(g)+2CO2(g)⇌4CO(g)+3H2(g) ∆H3=(-110 kJ∙mol-1)´4-(-84kJ∙mol-1)-( -393 kJ∙mol-1)´2=430 kJ∙mol-1。
②A.反应Ⅰ为吸热反应,升高温度能使其化学平衡向正反应方向移动,故其平衡常数增大,A正确;
B.反应Ⅰ和反应Ⅱ的正反应均为气体分子数增大的反应,增大压强,其化学平衡均向逆反应方向移动,B不正确;
C.反应Ⅲ的产物中有CO,增大CO的浓度,能使反应Ⅱ的化学平衡向逆反应方向移动,故其不利于乙烷脱氢,不利于乙烯的生成,C不正确;
D.反应Ⅳ的反应前后气体分子数不变,在恒温恒压下向平衡体系中通入水蒸气,体系的总体积变大,水蒸气的浓度变大,其他组分的浓度均减小相同的倍数,因此该反应的浓度商变大(大于平衡常数),化学平衡向逆反应方向移动,D正确。
综上所述,描述正确的是AD。
③由题中信息可知,反应Ⅱ分两步进行,第一步的反应是C2H6(g)+CO2(g)®C2H4(g)+H2(g) +CO2(g),C2H4(g)、H2(g)、CO2(g)的相对能量之和为52 kJ∙mol-1+0+(-393 kJ∙mol-1)= -341 kJ∙mol-1;第二步的反应是C2H4(g)+H2(g) +CO2(g)®C2H4(g)+H2O(g) +CO(g),其活化能为210 kJ∙mol-1,故该反应体系的过渡态的相对能量又升高了210 kJ∙mol-1,过渡态的的相对能量变为-341 kJ∙mol-1+210 kJ∙mol-1= -131 kJ∙mol-1,最终生成物C2H4(g)、H2O(g)、CO(g)的相对能量之和为(52 kJ∙mol-1)+(-242 kJ∙mol-1)+(-110 kJ∙mol-1)= -300 kJ∙mol-1。根据题中信息,第一步的活化能较小,第二步的活化能较大,故反应Ⅱ分两步进行的“能量—反应过程图”可以表示如下: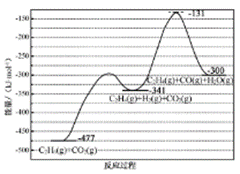 。
。
(2)①由题中信息及表中数据可知,尽管CO2和C2H6按物质的量之比1:1投料,但是C2H4的产率远远小于C2H6的转化率,但是CO2的转化率高于C2H6,说明在催化剂X的作用下,除了发生反应Ⅱ,还发生了反应Ⅲ,而且反应物主要发生了反应Ⅲ,这也说明催化剂X有利于提高反应Ⅲ速率,因此,CO2氧化C2H6的主要产物是CO。故答案为:CO;C2H4的产率低说明催化剂X有利于提高反应Ⅲ速率。
②由题中信息可知,选择性膜技术可提高C2H4的选择性,由反应ⅡC2H6(g)+CO2(g)⇌C2H4(g)+H2O(g) +CO(g)可知,该选择性应具体表现在选择性膜可选择性地让C2H4通过而离开体系,即通过吸附C2H4减小其在平衡体系的浓度,从而促进化学平衡向正反应方向移动,因而可以乙烷的转化率。故答案为:选择性膜吸附C2H4,促进反应Ⅱ平衡向正反应方向移动。
【点睛】本题“能量—反应过程图”是难点。一方面数据的处理较难,要把各个不同状态的相对能量算准,不能遗漏某些物质;另一方面,还要考虑两步反应的活化能不同。这就要求考生必须有耐心和细心,准确提取题中的关键信息和关键数据,才能做到完美。