光气(COCl2),又称碳酰氯,用于有机合成,制造染料、橡胶、农药、塑料等。实验室可利用CO与Cl2在活性炭催化下反应制取少量COCl2,实验装置如图所示。
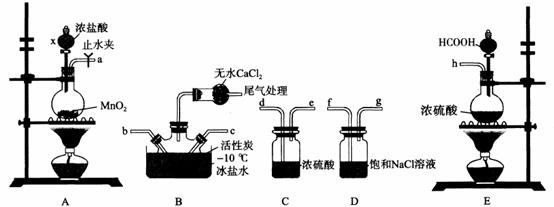
已知:光气常温下是一种略带黄色的气体,熔点为-118°C,沸点为8.2°C,密度为1.381 g·mL-1,它化学性质不稳定,遇水迅速水解,100°C以上易分解。
请回答下列问题:
(1)检查装置A气密性的操作为
(2)仪器x的名称为
(3)装置E中利用HCOOH制备CO的化学方程式为 。
(4)选择实验装置并连接接口(a~h)顺序:a- -b-c- -h(用小写字母表示,装置可重复使用)。
(5)Cl2还可用KMnO4和浓盐酸制备,其反应的离子反应方程式为 。
(6)装置B中-10°C冰盐水的作用为
答案


 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L