以干海带为原料提取碘单质和氯化钾的过程主要分三步:完成下列填空:
(1)步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在 (填写仪器名称)中加热,选用热水而不是冷水浸泡海带灰的目的是 。
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I-,制得富碘溶液。实验室模拟氧化过程的实验装置如图所示。
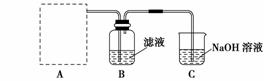
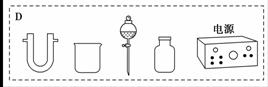
装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl-;二是电解法。限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是 (选填编号)。
a.2NaCl(s)+MnO2+2H2SO4(浓)![]() MnSO4+Cl2↑+Na2SO4+2H2O
MnSO4+Cl2↑+Na2SO4+2H2O
b.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
d.4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
广口瓶B中发生反应的离子方程式是 。装置C中NaOH的作用是 。
(3)步骤三:取100 mL B中富碘溶液,按如下流程分离碘单质。
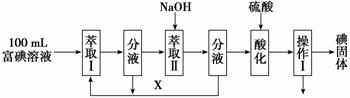
萃取Ⅱ和酸化过程发生的离子反应方程式分别是:
3I2+6OH-=5I-+IO![]() +3H2O; ;
+3H2O; ;
萃取剂X应选择 (选填编号)。
a.100 mL苯 b.10 mL乙醇 c.10 mL CCl4 d.10 mL己烯
实验室进行萃取操作的仪器是 。操作Ⅰ的名称是 。
(4)分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:①要用到的化学试剂是 (填写化学式);②要测定的物理量是 。
答案
(1)坩埚(1分) 加快溶解速率(1分)
(2)bc(2分) Cl2+2I-===I2+2Cl-(1分) 吸收未反应的氯气,防止污染(1分)
(3)5I-+IO![]() +6H+=3I2+3H2O(1分) c(1分) 分液漏斗(1分) 过滤(1分)
+6H+=3I2+3H2O(1分) c(1分) 分液漏斗(1分) 过滤(1分)
(4)①BaCl2或CaCl2(1分) ②样品质量和干燥沉淀质量(2分)


