Ⅰ.已知某可逆反应:aA(g)+bB(g) ![]() cC(g)+dD(g)。请回答下列问题:
cC(g)+dD(g)。请回答下列问题:

(1)根据实验测定结果,描绘出了该反应达到平衡状态时及改变外界条件后,反应速率与时间的关系图像(如图1所示),有利于提高D产量的变化过程是图像中的______段;引起该变化过程的外界条件是_________________________________________。
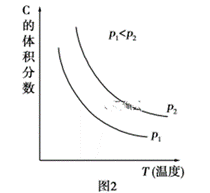
(2)根据实验测定结果描绘出了图2。由此图像可以得出,升高温度,上述平衡将向____(填“正反应”或“逆反应”)方向移动;反应计量数之间![]() 关系:a+b______c+d(填“大于”、“小于”、“等于”或“不确定”)。
关系:a+b______c+d(填“大于”、“小于”、“等于”或“不确定”)。
Ⅱ.工业合成氨反应如下:N2+3H2![]() 2NH3。请回答下列问题:
2NH3。请回答下列问题:
(1)在一定条件下2L的密闭容器中进行实验,并测得下列数据:
| 物质 | N2 | H2 | NH3 |
| 起始(mol) | 2 | 7 | 0 |
| 10s(mol) | 1.6 | ||
| 平衡时(mol) | 2 |
则10s内,用氢气表示的化学反应速率是______,该反应的化学平衡常数是________。
(2)根据混合气体各成分的物质性质,你认为工业上将氨气从混合气体中分离出来的措施是________,从而达到反应气体循环利用的目的。实验室检验氨气的方法是__________。
答案
【答案】 (1). t3~t4 (2). 增加反应物的浓度或增大A浓度或增大B浓度 (3). 逆反应 (4). 大于 (5). 0.12mol/(L·s) (6). 0.25 (7). 降温使NH3成为液体,与N2和H2分离开 (8). 用湿润的红色石蕊试纸靠近瓶口或试管口,弱试纸变蓝色,说明存在氨气
【解析】
【详解】I.(1)t3时刻改变的条件,只增加正反应速率,逆反应速率不变,即增加反应物的浓度,反应向正反应方向进行,即D的物质的量增大,t5时刻,反应向逆反应方向进行,消耗D,有利于提高D产量的变化过程是图像中的t3~t4;
(2)根据图像2,随着温度的升高,C的体积分数减小,说明平衡向逆反应方向进行,根据勒夏特列原理,该反应的正反应方向是放热反应,△H<0;等温下,压强增大,C的体积分数增大,即增大压强,平衡向正反应方向进行,a+b>c+d;
II.(1)10s内,生成NH3的物质的量为1.6mol,此时消耗H2的物质的量为![]() =2.4mol,根据化学反应速率数学表达式,v(H2)=
=2.4mol,根据化学反应速率数学表达式,v(H2)=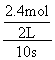 =0.12mol/(L·s);达到平衡时,n(NH3)=2mol,n(H2)=4mol,n(N2)=1mol,根据平衡常数的表达式,K=
=0.12mol/(L·s);达到平衡时,n(NH3)=2mol,n(H2)=4mol,n(N2)=1mol,根据平衡常数的表达式,K=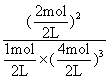 =0.25;
=0.25;
(2)NH3易液化,可以采用降温使NH3成为液体,与N2和H2分离开;NH3是中学阶段学过的唯一一种碱性气体,检验时可以采用用湿润的红色石蕊试纸靠近瓶口或试管口,弱试纸变蓝色,说明存在氨气。
