对于可逆反应A(g)+2B(g) ![]() 2C(g) ΔH>0,下列图像中正确的是( )
2C(g) ΔH>0,下列图像中正确的是( )
A.  B.
B. 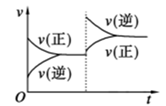
C. 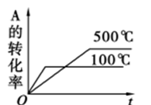 D.
D. 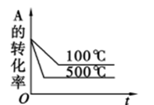
答案
【答案】B
【解析】
【详解】A、随着压强增大,化学反应速率加快,故A错误;
B、根据图像,改变条件![]() 那个时刻,v逆增大,v正不变,说明这一条件改变的是浓度,即增大生成物的浓度,故B正确;
那个时刻,v逆增大,v正不变,说明这一条件改变的是浓度,即增大生成物的浓度,故B正确;
C、温度高,反应速率增大,即500℃时先达到平衡,故C错误;
D、随着反应的进行,A的转化率增大,故D错误;
答案选B。
