.下列物质的水溶液呈碱性的是
A. CH3COOH B. CH3COONa C. CH3CH2OH D. NH4Cl
答案
【答案】B
【解析】
【分析】
判断物质在水溶液中的酸碱性,先分析物质是酸、碱还是盐,若为盐,再具体考虑水解对溶液酸碱性的影响,据此来分析作答。
【详解】A. CH3COOH属于酸,溶于水电离出H+,水溶液显酸性,故A项错误;
B. CH3COONa属于强碱弱酸盐,溶于水发生水解,CH3COO-+H2O![]() CH3COOH+OH-,
CH3COOH+OH-,
水解出OH-,溶液显碱性,故B项正确;
C. CH3CH2OH是非电解质,溶于水形成溶液时不能电离,水溶液显中性,故C项错误;
D. NH4Cl属于强酸弱碱盐,溶于水发生水解,NH4++H2O![]() NH3・H2O+H+,水解出H+,溶液显酸性,故D项错误。
NH3・H2O+H+,水解出H+,溶液显酸性,故D项错误。
答案选B。
【点睛】溶液酸碱性判断方法一,是根据H+与OH-浓度大小定量判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)=c(OH-)时,溶液呈中性;
当c(H+)<c(OH-)时,溶液呈碱性。
方法二,判断本身是酸、碱或者盐,若为盐,则再次判断该盐溶液是否发生水解。单一盐溶液,可根据“谁弱谁水解,谁强显谁性”原则判断;若为复杂酸式盐,单纯从酸式酸根离子考虑,则需要讨论其水解程度与电离程度的相对大小,如NaHCO3溶液中,HCO3-水解显碱性,电离显酸性,但其水解程度大于电离程度,故NaHCO3溶液整体表现为显碱性。

 ” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。 

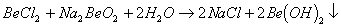 能完全进行,则下列推断中,正确的是
能完全进行,则下列推断中,正确的是 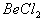 溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO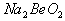 溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO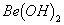 既能溶于盐酸又能溶于烧碱溶液
既能溶于盐酸又能溶于烧碱溶液