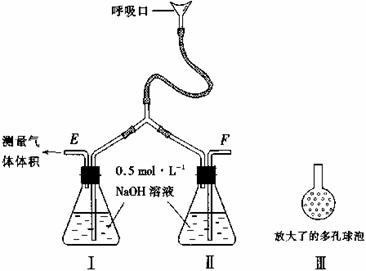
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式:
2NH3(g)+CO2(g)NH2COONH4(s) ΔH=-Q kJ·mol-1 (Q>0)
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。
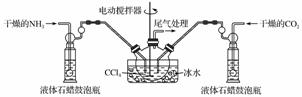
注:四氯化碳与液体石蜡均为惰性介质。
(1)发生器用冰水冷却的原因是___________________________________________________
____________________________________________________________(答两点)。
(2)液体石蜡鼓泡瓶的作用是__________________________________________________
________________________________________________________________________。
(3)从反应后的混合物中分离出产品的实验方法是________(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
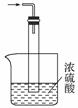
(4)尾气处理装置如图所示。浓硫酸的作用:______________________________________
________________________________________________________________________。
(5)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.782 0 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为________。
答案
答案 (1)降低温度提高反应物转化率;防止因反应放热造成产物分解;防止NH3和CO2逸出,增大NH3和CO2的溶解度(答出任意两点即可)
(2) 通过观察气泡,调节NH3与CO2通入比例为2∶1
(3)过滤 c
(4)吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解
(5)80.00%
解析 (1)生成NH2COONH4(s)的反应放热,降低温度平衡向正反应方向进行,有利于生成氨基甲酸铵。且氨基甲酸铵受热易分解,所以反应过程中需要用冰水冷却。(2)因为气体参与的反应不易控制反应速率和用量,所以液体石蜡鼓泡瓶的作用是控制反应进行程度,控制气体流速和原料气体的配比,即通过观察气泡,调节NH3与CO2通入比例。
(3)由制备氨基甲酸铵的装置图可知,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵晶体小,其晶体悬浮在四氯化碳中,分离产品的实验方法是过滤,氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、不能加热烘干,应在真空40 ℃以下烘干,所以答案选c。(4)氨气是碱性气体,浓硫酸是强酸,且具有吸水性,所以浓硫酸的作用是吸收多余的氨气,同时防止空气中水蒸气进入反应器使氨基甲酸铵水解。
(5)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.782 0 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。该物质是碳酸钙,其物质的量为1.000 g÷100 g·mol-1=0.010 mol。设样品中氨基甲酸铵的物质的量为x,碳酸氢铵的物质的量为y,依据碳原子守恒得到:x+y=0.01 mol,又因为78 g·mol-1·x+79 g·mol-1·y=0.782 0 g,解得x=0.008 mol、y=0.002 mol,则样品中氨基甲酸铵的物质的量分数=![]() ×100%=80.00%。
×100%=80.00%。

 2H2O
2H2O  2CO2 CO2+Ca(OH)2=CaCO3↓+H2O
2CO2 CO2+Ca(OH)2=CaCO3↓+H2O  NH3?H2O
NH3?H2O NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl
NH4++OH-;②用蘸浓盐酸玻璃棒靠近冒白烟:NH3+HCl==NH4Cl  CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O
CO2+2H2O CO2+Ca(OH)2==CaCO3↓+H2O  2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br
2CO2+2H2O ;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br  4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2
4CO2+2H2O;②使KMnO4(H+)溶液褪色;③使溴水褪色:CH≡CH+2Br2→CHBr2-CHBr2  的检验;
的检验;  的检验;
的检验;  苯酚的检验。
苯酚的检验。