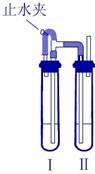
化合物M由两种元素组成,某研究小组按如图流程探究其组成:
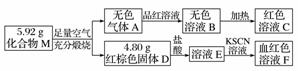
请回答:
(1)在制作印刷电路板的过程中常利用铜与溶液E反应,反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(2)将气体A通入溶液E中,溶液由黄色变成浅绿色,且酸性明显增强,写出该反应的离子方程式:________________________________________________________________________
________________________________________________________________________。
(3)化合物M的化学式为________。
答案
答案 (1)2FeCl3+Cu===2FeCl2+CuCl2 (2)2Fe3++SO2+2H2O===2Fe2++SO![]() +4H+
+4H+
(3)Fe3S4
解析 由A可使品红溶液褪色,加热又变红,可知无色气体A为SO2,由D为红棕色,与盐酸反应后加KSCN为血红色,可知E中含铁离子,D为Fe2O3,n(Fe2O3)=4.80 g÷160 g·mol-1=0.03 mol,M由Fe、S元素组成,n(Fe)=0.06 mol,n(S)=(5.92 g-0.06 mol×56 g·mol-1)÷32 g·mol-1=0.08 mol,M中Fe、S原子个数比为0.06 mol∶0.08 mol=3∶4,则M的化学式为Fe3S4。
(1)溶液E为氯化铁,则铜与溶液E反应的化学方程式为2FeCl3+Cu===2FeCl2+CuCl2。(2)气体A通入溶液E中,溶液由黄色变成浅绿色,且酸性明显增强,反应的离子方程式为2Fe3++SO2+2H2O===2Fe2++SO![]() +4H+。(3)由上述分析可知M的化学式为Fe3S4。
+4H+。(3)由上述分析可知M的化学式为Fe3S4。