为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂。
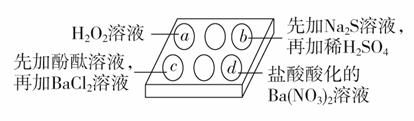
下列关于实验现象的解释或结论正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a中无明显现象 | Na2SO3和H2O2一定不发生反应 |
| B | b中加稀H2SO4后产生淡黄色沉淀 | SO |
| C | c中加BaCl2溶液后产生白色沉淀且红色褪去 | Ba2++SO |
| D | d中产生白色沉淀 | 原Na2SO3溶液中含有SO |
答案
答案 C
解析 亚硫酸钠具有还原性,滴入H2O2后,Na2SO3被H2O2氧化为硫酸钠,但没有明显的现象,A错误;B中是滴入硫化钠溶液和稀硫酸,硫离子和亚硫酸根离子发生氧化还原反应生成淡黄色沉淀单质硫,发生反应的离子方程式是:SO![]() +2S2-+6H+===3S↓+3H2O,但SO
+2S2-+6H+===3S↓+3H2O,但SO![]() 和S2-两种离子在碱性条件下不反应,能大量共存,B错误;在Na2SO3溶液中,SO
和S2-两种离子在碱性条件下不反应,能大量共存,B错误;在Na2SO3溶液中,SO![]() 水解显碱性:SO
水解显碱性:SO![]() +H2OHSO
+H2OHSO![]() +OH-,所以滴入酚酞后溶液变红,在该溶液中加入BaCl2后,Ba2++SO
+OH-,所以滴入酚酞后溶液变红,在该溶液中加入BaCl2后,Ba2++SO![]() ===BaSO3↓(白色),水解平衡左移,氢氧根离子浓度减小,红色褪去,C正确;无论原亚硫酸钠中是否含有SO
===BaSO3↓(白色),水解平衡左移,氢氧根离子浓度减小,红色褪去,C正确;无论原亚硫酸钠中是否含有SO![]() ,d中都会产生白色沉淀,D错误。
,d中都会产生白色沉淀,D错误。