硫单质及其化合物在化工生产、污水处理等领域应用广泛。
(1)煤制得的化工原料气中含有羰基硫(O=C=S),该物质可转化为H2S,主要反应如下:
i.水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g)△H1
H2S(g)+CO2(g)△H1
ⅱ.氢解反应:COS(g)+H2(g)![]() H2S(g)+CO(g) △H2
H2S(g)+CO(g) △H2
已知反应中相关的化学键键能数据如下表:
| 化学键 | H-H | C=O(COS) | C=S | H-S | C |
| E/kJ·mol-1 | 436 | 745 | 580 | 339 | 1076 |
①一定条件下,密闭容器中发生反应i,其中COS(g)的平衡转化率(a)与温度(T)的关系如图(a)所示。则A、B、C三点对应的化学反应速率大小顺序为_________(填标号)。
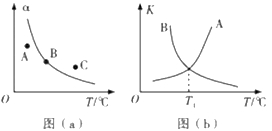
②结合上表中数据,计算反应ⅱ的△H2为___________。
③反应ⅱ的正、逆反应的平衡常数(K)与温度(T)的关系如上图(b)所示,其中表示逆反应的平衡常数(K)的曲线是_______________(填“A”或“B”)。T1℃时,向容积为2L的恒容密闭容器中充入2 mol COS(g)和1molH2(g),发生反应ⅱ,COS的平衡转化率为__________________。
(2)过二硫酸是一种强氧化性酸,其结构式如下所示,
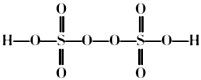 ,在Ag+催化作用下,S2O82-能与Mn2+在水溶液中发生反应生成SO42-和MnO4-,该反应的离子方程式为______。
,在Ag+催化作用下,S2O82-能与Mn2+在水溶液中发生反应生成SO42-和MnO4-,该反应的离子方程式为______。
(3)NaHS可用于污水处理的沉淀剂。
已知:25℃时,反应Hg2+(aq)+HS-(aq)![]() HgS(s)+H+(aq)的平衡常数K=1.75×1038,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15。则Ksp(HgS)=__________。
HgS(s)+H+(aq)的平衡常数K=1.75×1038,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15。则Ksp(HgS)=__________。
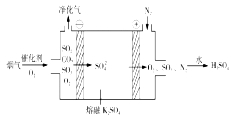
(4)降低SO2的排放量已经写入2018年政府工作报告,某种电化学脱硫法装置如下图所示,不仅可脱除烟气中的SO2,还可以制得H2SO4。在阴极放电的物质是_____________,在阳极生成SO3的电极反应式是__________________。
 。
。
答案
【答案】vA<vB<vC+7kJ/molB33.3%5S2O82-+2Mn2++8H2O![]()
10SO42-+2MnO4-+16H+4.0×10-53O2SO2-2e-+SO42-=2SO3
 成硫酸,这样,不仅可脱除烟气中的SO2还可以制得硫酸,在阴极放电的物质是O2,在阳极生成SO3的电极反应式是SO2-2e-+SO42-=2SO3。
成硫酸,这样,不仅可脱除烟气中的SO2还可以制得硫酸,在阴极放电的物质是O2,在阳极生成SO3的电极反应式是SO2-2e-+SO42-=2SO3。
